La materia siempre está sujeta a transformaciones, que pueden ser químicas o físicas. Las transformaciones químicas cambian la naturaleza de los compuestos que reaccionan, generando nuevas sustancias como productos, como quemar (o quemar) papel. Las transformaciones físicas, en cambio, son aquellas que no cambian la naturaleza del compuesto y no generan nuevas sustancias, como el acto de amasar el papel, o el derretimiento de los casquetes polares. En el último caso, lo que ocurre es una transformación física llamada cambio de estado físico.
Toda la materia se encuentra en algún estado físico y, dependiendo de las condiciones de presión y temperatura, puede pasar a otros estados. Este tipo de transformación se está produciendo todo el tiempo a nuestro alrededor, como, por ejemplo, en el hielo de nuestro vaso de jugo, que va de sólido a líquido, diluyendo el jugo y haciéndolo más «acuoso», o incluso, en el vapor presente en el aire que, al entrar en contacto con la superficie fría del vidrio, se convierte en líquido, formando gotas de agua alrededor del vidrio frío, dando la impresión de que el vidrio está “sudando”.
La transición del estado sólido al estado líquido se llama Fusión, o, como se le conoce popularmente, derretir. El hielo, tanto de las capas de hielo como de nuestro vaso de jugo, convertido en agua líquida es un ejemplo de fusión. Otros ejemplos que se pueden citar son la fusión de una vela encendida (fusión de parafina), inicio del proceso de fundición, en el que se calienta un metal sólido hasta que se vuelve líquido, para hacerlo moldeable, entre otros.
Para que una sustancia que se encuentra en estado sólido pase a líquido, es necesario suministrar energía a sus partículas. La energía aportada se convertirá en energía cinética, lo que provocará una mayor agitación entre las partículas y, en consecuencia, una mayor distancia entre ellas, caracterizando el estado líquido, en el que las fuerzas de atracción no son tan fuertes como en el estado sólido.
Por tanto, podemos decir que la fusión es un proceso endotérmico, es decir, absorbe energía y, por tanto, se produce cuando hay un aumento de temperatura. Cada sustancia tiene su punto de fusión, o temperatura bajo cierta presión, a la que cambia de sólido a líquido. En las sustancias puras es una determinada temperatura, que permanece constante durante toda la transformación, mientras que en las mezclas el cambio se producirá en un determinado rango, o intervalo, de temperaturas, y en ambas la presión se mantiene constante.
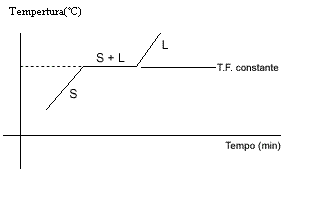
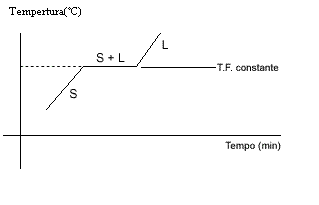
El gráfico muestra que la temperatura permanece estable durante la fusión de una sustancia pura.
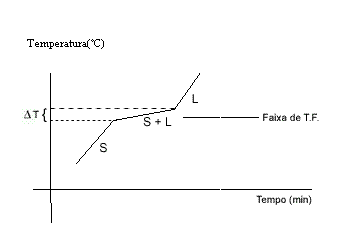
El gráfico muestra que la temperatura cambia al derretir una mezcla.
Las mezclas eutécticas, sin embargo, aunque sean mezclas, tienen un comportamiento diferente. Las mezclas eutécticas están formadas por determinadas sustancias, en determinadas proporciones, que hacen que la fusión de la mezcla sea similar a la de las sustancias puras: a una temperatura determinada y constante.
Cuando hay variación en la presión, la temperatura de fusión cambiará. Si la sustancia, en su estado sólido, tiene un volumen menor que en su estado líquido (como la gran mayoría de compuestos), es decir, cuando se funde, hay un aumento de volumen, al aumentar la presión, la temperatura de fusión, ya que tendrá su proceso obstaculizado, lo que requerirá que se produzcan temperaturas más altas. En el caso contrario, cuando la sustancia disminuye de volumen a medida que se derrite (como agua, hierro, antimonio, bismuto), un aumento de presión disminuirá la temperatura de fusión.