No hay límite de temperatura cuando comenzamos a calentar un material. Del estado sólido pasa al líquido, luego al gaseoso, se separa en moléculas, átomos, hasta llegar a una nube de partículas electrificadas, también llamada plasma, que se encuentra dentro de las estrellas, donde la temperatura es extremadamente alta. Sin embargo, hay un límite para el enfriamiento, es el cero absoluto! En una situación en la que la presión es cero, la temperatura no puede disminuir más y no se puede extraer más energía del material.
 El cero absoluto se define como la temperatura más baja que puede tener un cuerpo en el universo. Es la temperatura a la que las moléculas del cuerpo tienen energía cinética promedio cero (están en reposo). En teoría, sería 0K (cero en la escala Kelvin) o -273.15 ° C, pero en el laboratorio, el máximo que se alcanzó fue aproximadamente 0.000000000001K (o 1. 10-12 K).
El cero absoluto se define como la temperatura más baja que puede tener un cuerpo en el universo. Es la temperatura a la que las moléculas del cuerpo tienen energía cinética promedio cero (están en reposo). En teoría, sería 0K (cero en la escala Kelvin) o -273.15 ° C, pero en el laboratorio, el máximo que se alcanzó fue aproximadamente 0.000000000001K (o 1. 10-12 K).
Si el cero absoluto existiera en el valor exacto de 0, violaría el principio de incertidumbre de la mecánica cuántica, que establece que es imposible medir la posición y la velocidad simultáneamente, con absoluta precisión. Esto sucedería en el caso del cero absoluto, ya que la posición 0 y la velocidad 0 m / s se medirían simultáneamente.
Otro ejemplo de que el cero absoluto es inalcanzable se puede ver en el rendimiento (η) de una máquina de Carnot, dado por la ecuación:
η = 1 – Tfrío / Tcaliente
donde Tfrío es la temperatura de la fuente fría y Tcaliente la temperatura de la fuente caliente.
Si tfrío = 0K, es decir, cero absoluto, el rendimiento será del 100% (η = 1), situación en la que la máquina térmica convierte todo el calor en trabajo, algo imposible en un proceso cíclico en termodinámica.
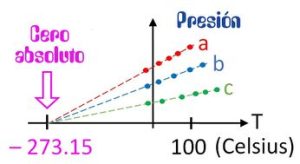
La medida del cero absoluto se obtuvo, en 1848, a partir de una propuesta de Lord Kelvin (1824-1907) cuando se dio cuenta de que la presión de un gas disminuía en la proporción de 1/273 de su valor inicial, cuando se enfriaba de 0ºC a – 1ºC, con volumen constante. Si en el cero absoluto la presión debe ser cero, porque sin energía cinética las moléculas están en reposo, la temperatura también lo estará, ya que registra el grado de agitación de las moléculas.
El mismo resultado se obtiene manteniendo la presión constante y enfriar el cuerpo de 0ºC a -1ºC, donde el volumen disminuye en una proporción de 1/273 del valor inicial, llegando a un volumen cero en el cero absoluto, lo cual es imposible.
En este razonamiento, Kelvin concluyó, para el cociente 1/273 encontrado, que el cero absoluto sería -273ºC, porque la razón es la diferencia de 1ºC.
Hay tres fenómenos que se observan en un cuerpo, cuando está cerca del cero absoluto:
superconductividad: el cuerpo crea un campo magnético tan grande que le permite levitar un imán;
superfluidez: debido a que la resistencia mecánica es casi nula, fluye tan bien que un líquido puede trepar por las paredes de un recipiente;
Condensación de Bose-Einstein: el cuerpo se está compactando, condensándose, de una manera que podría convertirse en un solo átomo grande. Este fenómeno se observa en los procesos de caída de temperatura y cambios de estado físico, en los que el gas se vuelve líquido, el líquido se vuelve sólido y, de esta manera, el sólido tendería a tener sus partículas cada vez más unidas.
Referencias bibliográficas:
HEWITT, Paul G., Física conceptual – 9ª ed. – Bookman, 2008.





