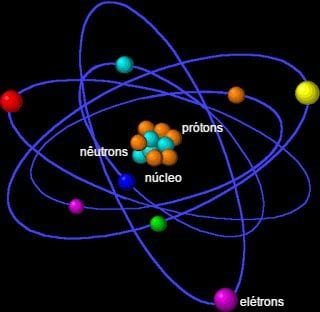
El modelo atómico de Rutherford sugiere que el átomo tiene la apariencia de un sistema planetario. Por eso se llama modelo planetario o de modelo en átomo nucleado.
Según este modelo presentado en 1911, los electrones giran alrededor del núcleo (formado por protones y neutrones), de manera similar a los planetas que giran alrededor del Sol.
Este modelo reemplazó al propuesto por Thomson en 1903. Antes, sin embargo, ya habían aparecido otros modelos atómicos sobre la distribución de partículas atómicas.
El modelo de Rutherford representa una revolución en este tema y se ha convertido en la base de la teoría atómica.
El experimento de Rutherford
En 1910, Rutherford (1871-1937) estaba estudiando la trayectoria de las partículas y la interacción entre la radiación alfa y los materiales. En esa ocasión, detectó que existía una limitación en el modelo atómico presentado por Thomson, el Modelo Atómico de Thomson.
Rutherford hizo una cámara de metal cerrada y colocó un pequeño recipiente de plomo con fragmentos de polonio.
Frente a este recipiente que tenía una abertura, colocó una hoja de oro muy delgada cubierta con una película de sulfuro de zinc.
Todo esto se conectó a un microscopio que podía girar 360º alrededor del portaobjetos de oro. El objetivo fue analizar la incidencia de partículas que penetraron a través de la hoja y se desintegraron espontáneamente a partir de elementos radiactivos naturales.
Fue posible ver la incidencia de cada partícula bajo la película de sulfuro de zinc a través de un punto resaltado en el microscopio.
Rutherford notó la incidencia de partículas en los ángulos más diversos para poder analizar cuidadosamente su comportamiento.
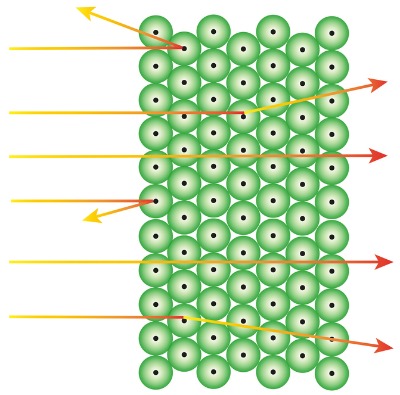
A partir de su análisis, Rutherford descubrió que el comportamiento de las partículas estaba estandarizado. La mayoría consiguió atravesar la sábana (aunque con cierta dificultad), otros quedaron bloqueados, mientras que algunos aún no se vieron afectados.
Rutherford concluyó que había muchos espacios vacíos y que el centro del átomo era mucho más pequeño considerando todo su diámetro. Entonces, descubrió la electrosfera. Es decir, el átomo estaba formado por un núcleo, donde había una carga positiva concentrada, y por una electrosfera, donde se concentra la carga negativa.
Rutherford no sabía de qué estaba hecho el núcleo. Simplemente asumió que había neutrones, pero eso solo se probó en la década de 1930.
Los electrones, a su vez, ya descubiertos por Thomson en 1905, están ubicados en la electrosfera y circulan alrededor de este pequeño sol nuclear.
Conozca la evolución de los modelos atómicos.
Fallo del modelo de Rutherford
A pesar de los avances, el modelo presentó un error, que se señala a través de la teoría del electromagnetismo.
Las partículas cargadas eléctricamente emiten una onda electromagnética cuando se aceleran. Siguiendo el modelo de Rutherford es lo que le pasaría al electrón que, en este caso, perdería energía y caería sobre el núcleo, pero no es lo que pasa.
El modelo atómico siguió evolucionando y Niels Bohr completó la brecha que existía en el modelo de Rutherford. Por esta razón, este modelo se denomina modelo atómico de Rutherford-Bohr.
Pon a prueba tus conocimientos sobre el tema en: ejercicios sobre modelos atómicos.





