La electronegatividad es un propiedad periódica que indica la tendencia del átomo a atraer electrones.. Ocurre cuando el átomo está en un enlace químico covalente, es decir, en el intercambio de uno o más pares de electrones.
Lo que lo determina es la capacidad del núcleo atómico para atraer electrones vecinos. A partir de ahí, según la teoría del octeto, se forman moléculas estables.
La electronegatividad se considera la propiedad más importante de la tabla periódica. Su importancia radica en el hecho de que induce el comportamiento de los átomos, a partir de los cuales se forman las moléculas.
Las otras propiedades periódicas son:
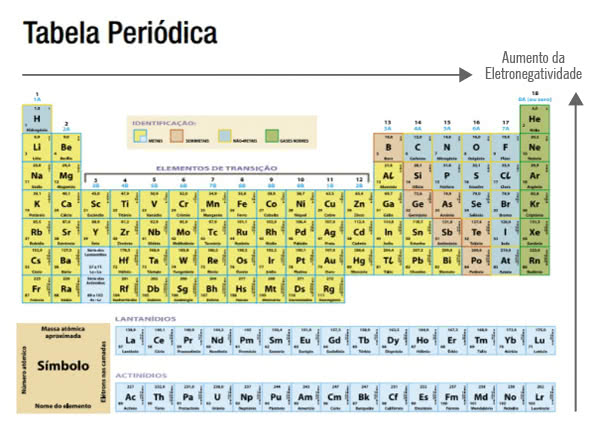
Variación de la electronegatividad en la tabla periódica
Los elementos más electronegativos se encuentran en el lado derecho y en la parte superior de la tabla periódica.
A medida que los elementos se alejan de esta posición, es decir, cuanto más se alejan hacia el lado izquierdo y hacia abajo, menos electronegativos son.
El flúor (F) es el elemento químico más electronegativo. Aunque no es el elemento que más se posiciona en el lado derecho de la mesa, es el primero justo después de los gases nobles.
Los gases nobles no forman enlaces químicos y, por esta razón, su electronegatividad es muy insignificante.
Mientras tanto, el cesio (Cs) y el francio (Fr) son los elementos menos electronegativos.
Lo contrario es cierto para el tamaño del radio atómico. Así, se puede decir que cuanto mayor es el radio atómico, menor es la electronegatividad de un elemento.
Lea también:
¿Qué es la electropositividad?
La electropositividad es la tendencia de los átomos a ceder electrones.
También se le conoce como carácter metálico porque los metales son los elementos más electropositivos.
En la electropositividad, se pierden electrones, lo que hace que la carga de los átomos sea positiva.
En la electronegatividad, a su vez, se agregan electrones a los átomos. Pronto, su carga se vuelve negativa.
¡Continúe su búsqueda! Leer: