Tabla de contenidos
Tú elementos radiactivos son elementos capaces de emitir radiación, que corresponde a ondas electromagnéticas que interactúan con la materia, produciendo diferentes efectos.
La radiactividad se descubrió a finales del siglo XIX y es un factor muy importante para ampliar el conocimiento sobre los elementos radiactivos, así como la estructura atómica de los átomos (formados por protones, neutrones y electrones).
A través del modelo atómico de Rutherford, presentado en 1911, los electrones se mueven en órbitas circulares alrededor del núcleo del átomo.
Clasificación
La radiactividad puede ser natural, encontrada en elementos que están dispuestos en la naturaleza, o artificial, mediante la creación de elementos radiactivos en el laboratorio.
radiactividad natural
La radiactividad natural observada en los isótopos radiactivos que se producen espontáneamente en la naturaleza se forma a partir de tres radionucleidos: uranio-238, uranio-235 y torio-232. Estos elementos inician las series o familias radiactivas.
serie radiactiva
Una serie de radiactividad es una secuencia de radioisótopos naturales que se producen espontáneamente por desintegraciones radiactivas sucesivas hasta que el último elemento de la serie es estable.
Para las tres familias, el último elemento es el plomo, en forma de diferentes isótopos.
Los elementos presentes en la serie natural son los isótopos de: uranio, torio, radio, protactinio, actinio, francio, radón y polonio.
Otros elementos que presentan radiactividad, aunque en mínima cantidad, en la naturaleza son: tritio (hidrógeno con masa 3u), carbono-14 y potasio-40.
Radiactividad artificial
Son los elementos producidos artificialmente por la transformación nuclear de un elemento formando otro elemento, principalmente por reacciones de transmutación.
En la transmutación, los átomos de los elementos son bombardeados por partículas aceleradas, produciendo un radioisótopo natural o artificial en el choque.
Ejemplo:
La primera transmutación artificial fue realizada por Rutherford en 1919, quien logró sintetizar oxígeno artificial.
Al bombardear átomos de nitrógeno con partículas alfa emitidas por el elemento polonio, se formó un elemento inestable, representado por y luego dio lugar a oxígeno y un protón.
Elementos transuránicos
Mediante reacciones nucleares, se pueden crear elementos artificiales.
Los elementos transuránicos de la tabla periódica fueron sintetizados en el laboratorio y tienen un número atómico mayor que el del uranio (Z 92), elemento con mayor número atómico encontrado en la naturaleza.
Los dos primeros elementos de esta serie, neptunio y plutonio, fueron producidos en 1940 por los científicos estadounidenses Edwin Mattison McMillan y Glenn Theodore Seaborg.
En general, estos elementos son de corta duración, hasta fracciones de segundo.
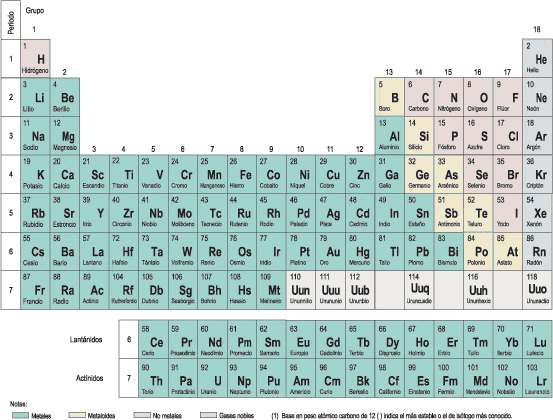
Elementos radiactivos de la tabla periódica
Recuerde que los radioisótopos son isótopos radiactivos. Aproximadamente 90 elementos radiactivos están presentes en la tabla periódica. Recuerde que los isótopos son átomos del mismo elemento químico y que tienen el mismo número atómico (Z) y diferente número de masa (A).
Elementos radiactivos principales
- Carbono (C)
- Cesio (Cs)
- Cobalto (Co)
- Estroncio (Mr)
- Yodo (I)
- Plutonio (Pu)
- Polonio (Po)
- Radio (Ra)
- Radón (Rn)
- Torio (Th)
- Uranio (U)
Elementos radiactivos y sus aplicaciones
Los elementos radiactivos tienen varias aplicaciones (medicina, agricultura, ingeniería, etc.) de las que destacan las siguientes:
- Producción de bombas nucleares
- Uso de la energía nuclear para la producción de electricidad.
- Esterilización y conservación de alimentos
- Determina la edad de fósiles y momias.
- Tratamiento de tumores
Energía nuclear
La energía nuclear, producida en centrales nucleares, utiliza elementos radiactivos (principalmente uranio) para producir electricidad.
Ha sido una alternativa para la generación de energía ya que es más económica y aún utiliza fuentes de energía limpia que no causan gran impacto ambiental.
Sin embargo, cuando ocurre un accidente, puede afectar considerablemente al medio ambiente. Un gran ejemplo es el accidente de Chernobyl que ocurrió en Ucrania en 1986. La población que vivía cerca se vio obligada a trasladarse como resultado de la liberación de radiación.
Polución radiactiva
La contaminación radiactiva corresponde a la contaminación producida por materiales radiactivos. El tipo de residuo generado se denomina residuo radiactivo o nuclear.
Profundiza tus conocimientos leyendo los textos: