Los materiales sólidos pueden ser cristalinos o amorfos. El concepto de estructura cristalina está relacionado con la organización de los átomos en forma geométrica.
Las estructuras cristalinas están presentes en varios materiales, en los que los átomos distribuidos dentro de su estructura forman una red denominada red cristalina. Por tanto, las sales, los metales y la mayoría de los minerales tienen estructuras cristalinas.
Las moléculas de las estructuras cristalinas pueden tener dos tipos de enlaces, los direccionales, que incluyen los enlaces covalentes y dipolo-dipolo, y los no direccionales, que incluyen los enlaces metálicos, iónicos, de van der Walls.
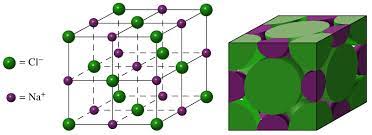
Las estructuras cristalinas están formadas por células unitarias que son su unidad básica, ya que constituyen el conjunto más pequeño de átomos asociados que se encuentran en una estructura cristalina.
Hay siete tipos de sistemas cristalinos que engloban sustancias conocidas por el hombre:
- Cúbico: donde todos los ángulos son iguales a 90º
- Tetragronal: donde todos los ángulos son iguales a 90º
- Ortorrómbico: donde todos los ángulos son iguales a 90º
- Monoclínico: donde hay dos ángulos iguales a 90º y dos ángulos diferentes a 90º
- Triclínico: donde todos los ángulos son diferentes y ninguno es igual a 90º
- Hexagonal: donde dos ángulos son iguales a 90 ° y un ángulo es igual a 120 °
- Romboédrico: donde todos los ángulos son iguales pero diferentes de 90 °.
Para cada posible ubicación de átomos, iones o moléculas en ciertos puntos, existe una clasificación de estructuras cristalinas en las redes de Bravais. Así, se puede representar mediante una tabla con datos de una de las siete clasificaciones anteriores, según el material elegido.
La transformación de líquido a sólido es característica de los elementos metálicos, adquiriendo la apariencia de estructuras densas, como la cúbica con cuerpo centrado.
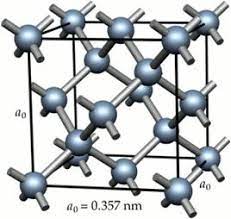
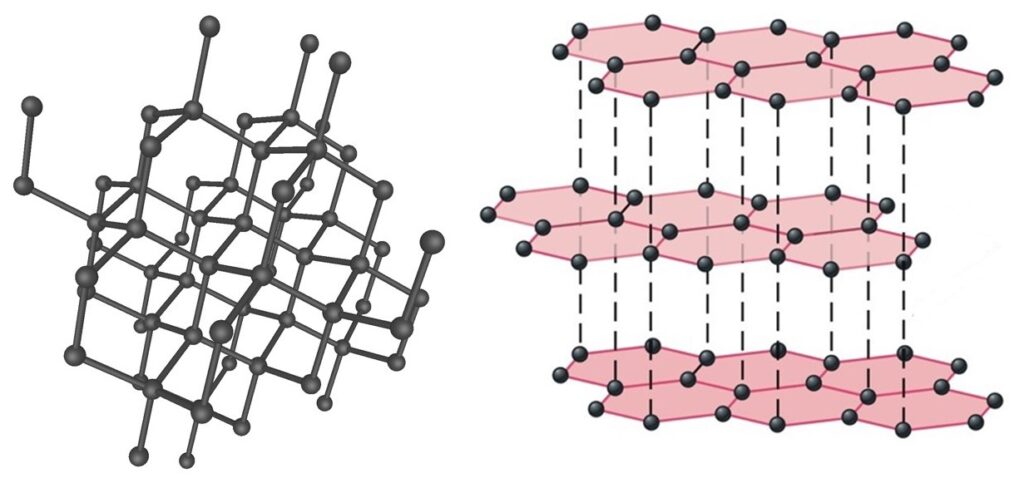
Cuando un mismo elemento o compuesto químico tiene diferentes formas cristalinas según las condiciones de presión y temperatura, este fenómeno se denomina polimorfismo. Como ejemplo, está el Hierro (Fe), que puede presentar las estructuras CFC (Cristalino Cúbico con Caras Centradas) y CCC (Cristalino Cúbico con Cuerpo Centrado), aspecto que debe ser considerado en su uso, como en procesos metalúrgicos. El carbono es también un ejemplo de elemento polimórfico, presente en el diamante, que es una estructura extremadamente dura, y también en el grafito, que es frágil.
La mayor parte del conocimiento sobre las estructuras cristalinas se adquiere mediante técnicas de rayos X, lo que permite obtener información sobre la ubicación correcta de cada átomo.
Las estructuras cristalinas tienen características como la piezoelectricidad, que es la capacidad de generar una corriente eléctrica si existe algún tipo de presión mecánica; ferroelectricidad que, si bien no conducen corriente eléctrica, de acuerdo con su temperatura, desarrollan una polarización espontánea, que puede revertirse, posibilitando el uso de un campo eléctrico externo; Efecto piroeléctrico en el que el aumento de temperatura provocará una polarización espontánea, en el que se puede aprovechar el campo eléctrico generado en la superficie del material y son semiconductores.
Debido a estas propiedades, los materiales con estructuras cristalinas son ampliamente utilizados por la industria en la fabricación de termómetros, transistores, cámaras, relojes y básculas.
Existen varios procesos de cristalización en el universo mineralógico y, por tanto, tendremos diversificaciones en el cristales formado. El entorno químico (composición química), la temperatura y la presión del lugar donde se forman los minerales es un factor limitante en la formación de cristales.
Llamamos elementos minerales o compuestos químicos que se formaron en condiciones geológicas naturales, presentando así una composición química y propiedades cristalográficas definidas. Son estos parámetros los que se utilizan para definir un cristal, ya que se forman en ambientes geológicos ideales y por tanto presentan una serie de propiedades únicas entre los minerales (aparición de caras geométricas, aristas y vértices en el cuerpo rocoso).
Cristalografía
La cristalografía estudia el origen y formación de los cristales, clasificándolos. Se deben observar los siguientes criterios para permitir la caracterización de los cristales:
- Composición química del mineral.
- Cristalización interna y externa
- proceso de formación geoquímica
- Proceso de formación inorgánica
La composición química del mineral indica sus elementos químicos, representados por los coeficientes de ciertos átomos en la fórmula general del mineral. Por ejemplo, los minerales que contienen el anión silicato (SiO44-) se referirá a la clase de silicatos y aniones nitrato (NO3–) al grupo de los nitratos. Esta clasificación permite la agrupación por la naturaleza de la composición química del mineral y, por tanto, del cristal analizado.
Los procesos de cristalización definen propiedades importantes de los cristales: red cristalina, hábito cristalino y escisión. Ambos dependen de las condiciones de formación del mineral, que es un factor determinante en la formación de cristales. Los cristales necesitan ambientes geológicos “tranquilos” para crecer y desarrollarse, exhibiendo las cualidades que los definen.
Red cristalina se refiere a la estructura atómica que presenta el mineral y su organización de los átomos en el espacio tridimensional, obedeciendo los preceptos de la simetría cristalográfica (simetría en la distribución de los átomos del mineral en relación al plano simétrico central). Cuando esta celosía se forma en ambientes ideales, influye en el hábito del cristal, la forma geométrica exterior natural del cristal. Los cristales de halita (NaCl) tienen un hábito cristalino cúbico centrado en el cuerpo y experimentan escisión (rotura) en los planos que tienen los enlaces químicos más débiles. Pronto, tus cristales serán cúbicos.
Los sistemas cristalinos se clasifican de manera que permitan la identificación previa del nivel organizativo de la estructura interna del mineral, partiendo del cúbico, de mayor simetría, al triclínico, de menor simetría.
| sistema de cristal | Minerales |
| Cúbico | Diamante *, granate, halita |
| Tetragonal | Rutilo, casiterita |
| Hexagonal | Berilo, cuarzo β, grafito * |
| Trigonal | Turmalina, corindón, cuarzo α |
| Ortorrómbico | Topacio, olivino, azufre * |
| Monoclínica | Mica, ortoclasa, azufre * |
| triclínico | Plagioclasa, microclina |
Cuadro adaptado del libro: Descifrando la Tierra – cap. 2 Minerales y rocas. p.31.
* variaciones de cristales con el mismo elemento químico
La química, a través de estudios de alotropía, observa las propiedades de minerales que tienen la misma composición química, como el diamante y el grafito (formado por carbono).
El proceso de formación geoquímica nos remite a los procesos utilizados para formar el cristal, difiriendo entre dos formas posibles: natural o sintético. Los minerales y cristales formados naturalmente ocurren espontáneamente en el medio ambiente, mientras que sus contrapartes sintéticas no se llaman minerales, aunque tienen todas sus propiedades.
El proceso de formación de minerales inorgánicos delimita solo los procesos geoquímicos como formadores de minerales. Los procesos que se originan en los seres vivos (formación de ámbar, perla) no se consideran procesos inorgánicos y sus productos se denominan mineraloides.
Fuentes:
NEVES, Paulo Cesar Pereira. Introducción a la mineralogía práctica.
BUNN, CW – Cristales: su papel en la naturaleza y la ciencia