Tabla de contenidos
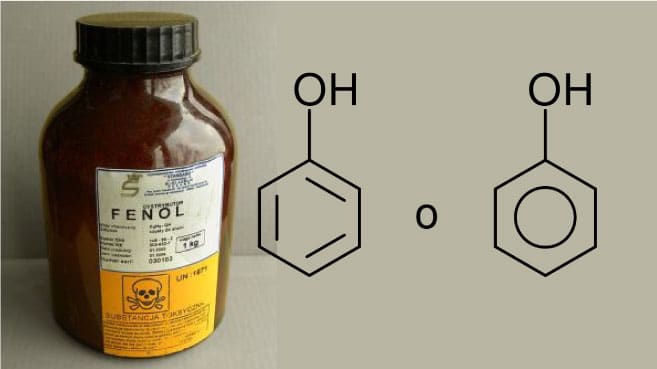
El Fenol es una función orgánica, es decir, está formada por compuestos orgánicos (presencia de átomos de carbono), caracterizada por la presencia del grupo funcional hidroxilo (-OH) junto con el anillos de benceno (carbono con núcleo de benceno) o aromáticos (C6H6).
El grupo fenol tiene una fórmula molecular C6H5OH, y también se denominan: hidroxibenceno, monohidroxi, benceno, benceno, fenol común o ácido carbólico. Sin embargo, los fenoles son solubles en alcohol y éter y son poco solubles en agua, siendo obtenidos mediante la extracción de aceites (alquitrán de hulla), hojas y pétalos de algunas plantas (carqueja, jengibre, clavo, orégano, tomillo). Además, estos compuestos orgánicos tienen las siguientes características: sustancia cristalina (sólida), incolora (mayoritariamente), ácida, de olor fuerte e irritante,
Por tanto, cabe destacar que gran parte de los fenoles se consideran peligroso por ser altamente corrosivos, tóxicos, irritantes para las mucosas, provocando quemaduras y, si se ingieren o inhalan, pueden provocar la muerte; en este caso, incluye la fabricación de explosivos, resinas, polímeros, pinturas, barnices y también bactericidas y fungicidas, por ejemplo, creolina (desinfectante). Sin embargo, vale la pena señalar que los fenoles son compuestos que también se utilizan ampliamente en las industrias de cosméticos, perfumes y tintes.
Nomenclatura de fenoles
La nomenclatura de los fenoles se realiza utilizando la palabra hidroxibenceno, precedido por sus posibles sustituyentes, o simplemente fenol. En anillos aromáticos ramificados, es común utilizar la siguiente designación para las posiciones de las ramas:
Los fenoles en general son mucho más ácidos que los alcoholes porque la sal resultante (fenolato o fenóxido) se estabiliza por resonancia de anillo (deslocalización de electrones). La deslocalización de los pares de electrones de oxígeno dentro del anillo aromático hace que estos compuestos no se comporten como una base como es posible para los alcoholes.
Como el hidroxilo es un orientador orto-director, en las reacciones de sustitución de los hidrógenos del anillo fenólico, las sustituciones siempre se producirán en estas posiciones.
Algunos fenoles importantes
Fenol (hidroxibenceno o ácido carbólico): es un sólido blanco que en lugares muy calientes presenta un aspecto ‘húmedo’. Fue el primer antiséptico utilizado en hospitales para prevenir la proliferación de microorganismos (hacia 1870). Su uso hoy como antiséptico está prohibido porque es muy corrosivo y provoca graves quemaduras.
Creoline: los metil-fenoles se conocen comúnmente como cresoles y la mezcla de isómeros orto, meta y para-cresol se usa ampliamente como desinfectante doméstico. Son sólidos blancos cuando se aíslan, pero en la mezcla de los isómeros de 3 posiciones se vuelven líquidos. Los cresoles a menudo huelen a medicamentos. Puede utilizarse en la fabricación de resinas sintéticas o modificadas para su aplicación en electrónica.
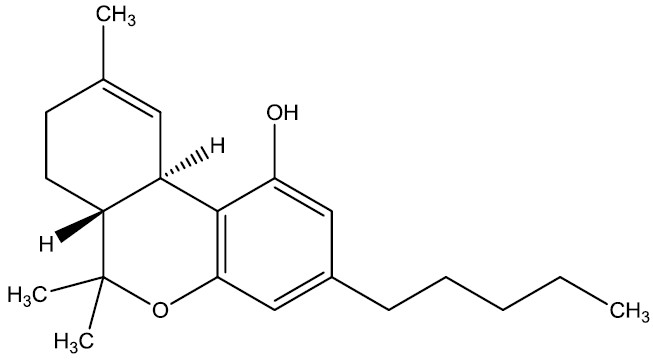
THC (tetrahidrocannabinol): es la principal sustancia psicoactiva que se encuentra en las plantas del género canabis. Puede obtenerse por extracción de esta planta o por síntesis de laboratorio. A diferencia del alcohol, el THC permanece en la sangre durante aproximadamente ocho días y puede detectarse mediante análisis de sangre. Por este motivo, el consumo de marihuana a intervalos inferiores a ocho días provoca un aumento de la concentración de THC en sangre.
Baquelita: es una resina sintética, obtenida por polimerización de fenol con formaldehído, químicamente estable y resistente al calor. Es resistente al calor, infusible y fuerte, se quema lentamente, se puede laminar y moldear en la fase inicial de su fabricación, es de bajo coste y se puede incorporar en barnices y lacas. Su uso ha disminuido mucho, ya que es frágil, pero aún se utiliza en materiales que necesitan ser resistentes a las temperaturas, como portalámparas y mangos de ollas.
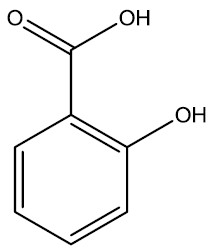
Ácido salicilico: Se utiliza como exfoliante en tratamientos de psoriasis y dermatitis exfoliantes. También es el precursor de la síntesis de ácido acetilsalicílico (AAS) y salicilato de metilo. Puede producirse acidificando una solución que contenga salicilato de sodio. Cuando es puro, el ácido salicílico es un polvo cristalino blanco, inodoro y escasamente soluble en agua.
Bibliografía:
Clasificación de fenoles
Según la cantidad de hidroxilos presentes en la molécula, los fenoles se clasifican en:
- Monofenoles: molécula formada por un hidroxilo
- Difenoles: molécula formada por dos hidroxilos
- Trifenoles: moléculas formadas por tres hidroxilos
Ejemplos de fenol
- cresol: Se encuentran en gran parte en la naturaleza (alimentos, madera, humo de tabaco, alquitrán de hulla), los cresoles se utilizan para conservar la madera a través de su poder repelente, en la producción de antisépticos, tintes, perfumes, insecticidas, resinas, generadores, explosivos, solventes, entre otros. ; son conocidos popularmente por los nombres: creoline y lysol. Existen tres tipos de cresoles: Orthocresol (O-Cresol), Metacresol (M-Cresol) y Paracresol (P-Cresol), con fórmula molecular: C7H8O.
- hidroquinona: Conocido como quinol, este fenol se ha utilizado ampliamente en tratamientos para la piel, como el peeling. Además de la medicina, la hidroquinona se usa en la producción de polímeros, herbicidas y antioxidantes; su fórmula molecular es C6H6O2.
- Eugenol: Conocido como aceite de clavo, el eugenol tiene propiedades antisépticas, anestésicas, medicinales y bactericidas. Está presente en el clavo, la canela y la mirra, y también es un compuesto muy utilizado por la industria cosmética; su fórmula molecular es: C10H12O2.
- Ácido pícrico: Conocido como trinitrofenol, este fenol es ácido y fuerte, se utiliza en la producción de drogas así como en la producción de granadas, bombas, armas, polímeros y cohetes; su fórmula molecular C6H3N3O7.
- Tú Compuestos fenólicos se forman a partir de la sustitución de uno o más átomos de hidrógeno por un grupo hidroxilo (OH–) en la molécula de benceno. El compuesto fenólico más simple es el fenol, que en realidad es el nombre específico del hidroxibenceno.
Algunos Compuestos fenolíticos
Benceno.
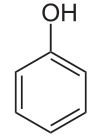
Hidroxibenceno.
Figura 1: estructuras de benceno e hidroxibenceno
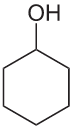
Se debe tener cuidado, ya que no todos los compuestos que contienen OH– unido a una cadena de carbono cerrada hay un fenol, ya que esta silla debe ser un anillo aromático. Tenga en cuenta la estructura a continuación, este compuesto no se considera un fenol, sino un alcohol, ya que el anillo es un ciclohexano, y esta sustancia se llama ciclohexanol.
Figura 2: Estructura del ciclo del hexanol
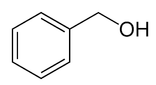
Otra observación importante es que el ion OH–debe fijarse directamente al anillo de benceno. La siguiente sustancia, por ejemplo, aunque tiene un hidroxilo y un anillo aromático, no es un fenol, ya que tiene un átomo de carbono entre el hidroxilo y el benceno.
Figura 3: alcohol bencílico
La nomenclatura de los fenoles sigue la regla utilizada para nombrar bencenos monosustituidos. En el caso de los monosustituidos, el nombre benceno se usa junto con el prefijo del sustituyente, como en el ejemplo de hidroxibenceno.
Además del hidroxilo, se pueden unir otros radicales al anillo aromático. Cuando tenemos dos sustituyentes, deben tener sus posiciones relativas al hidroxilo indicadas por los prefijos orto (o), meta (m) y para (p), o indicadas por números, como en las siguientes estructuras.
Figura 4: Moléculas de 4-clorofenol (PAG-clorofenol), 2-metilfenol (O-metilfenol) y 3-bromofenol (metro-bromofenol)
Los compuestos como el o-metilfenol también se denominan cresoles, en cuyo caso la nomenclatura sería o-cresol. Los compuestos que tienen dos hidroxilos se denominan bencenodioles, en cuyo caso la posición de los dos hidroxilos debe indicarse con números.
Figura 5: Moléculas de 1,2-bencenodiol y 1,4-bencenodiol
Los compuestos anteriores también se conocen comúnmente como catecol e hidroquinona.
Cuando tenemos un hidroxilo unido a un anillo benzoico policíclico, tenemos naftoles y fenantroles, que son químicamente similares a los fenoles.
Síntesis de algunos compuestos fenol
Obtención de tribromofenol
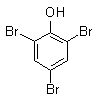
Fórmula estructural de tribomofenol
Los compuestos aromáticos, incluidos los fenoles, presentan una serie de reacciones características, llamadas reacciones aromáticas: halogenación, nitración y sulfonación.
La tribrominación del fenol se lleva a cabo fácilmente mediante la reacción de soluciones acuosas de fenol y una solución acuosa de bromo (agua de bromo). El tribromofenol formado precipita ya que es escasamente soluble en agua y puede aislarse por filtración. El tribromofenol se purifica disolviéndolo en alcohol etílico y cristalizando en alcohol / agua.
- Coloque 10 ml de solución de fenol en el vaso de precipitados.
- Agregue agua con bromo, con agitación, en pequeñas porciones, hasta que persista el color ligeramente amarillo (alrededor de 50 mL). Observe la precipitación de tribromofenol.
- Filtrar el tribromofenol formado.
- Lavar el precipitado con una pequeña cantidad de agua.
- Transferir el tribromofenol al matraz Erlenmeyer.
- Agregue 10 ml de alcohol etílico. Revuelva hasta que el tribromofenol se disuelva.
- Agregue 10 ml de agua a la solución alcohólica. Observe la lenta cristalización del tribromofenol.
- Filtrar el tribromofenol cristalizado.
- Almacene el producto en una botella debidamente limpia y etiquetada.
Síntesis de ácido pícrico
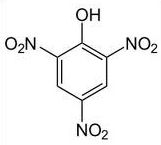
- Coloque una punta de espátula de fenol puro (aproximadamente 1 g) en un matraz Erlenmeyer de 100 ml y agregue 1,5 ml de HdosSOLO4 enfocado. Agitar y llevar a baño maría hirviendo durante 10 minutos. Después de enfriar, agregue 4 ml de HNO3 concentrar y dejar en la campana hasta que la reacción comience a procesar, lo que se puede observar por la liberación de vapores nitrosos.
- Cuando la intensidad de la reacción disminuya, caliéntela al baño maría hirviendo durante 30 minutos.
- Enfriar y agregar 10 ml de agua helada, dejando en un baño de hielo hasta que se obtenga la precipitación de ácido pícrico.
- Filtrar, lavando los cristales ácidos con porciones de agua helada.
Toxicidad del Fenol
Los fenoles, a diferencia de los alcoholes (compuestos que tienen -OH ligado a carbono saturado, sin comportamiento ácido) y enoles (compuestos que tienen -OH ligado a carbono insaturado, en cadena abierta), son compuestos que tienen uno o más grupos –OH unidos a la anillo de benceno. Tienen una fórmula general de Ar-OH. Se encuentran en el alquitrán de carbón y madera. Se utilizan como desinfectantes y germicidas, en la conservación de la madera, en la producción de explosivos, perfumes, en la fabricación de reveladores fotográficos y antioxidantes. Suelen aparecer como sólidos cristalinos. Cuando son puros, son incoloros y pueden tener un color rosado porque se oxidan fácilmente. Tienen un olor fuerte característico.
Tienen puntos de fusión y ebullición más altos que los compuestos de peso molecular similar, sin el grupo oxihidrilo, debido a los enlaces intermoleculares por enlaces de hidrógeno, como se muestra en la siguiente tabla:
El fenol común también se llama hidroxibenceno o ácido fenólico. Se presenta en forma de cristales y tiene un olor característico. Es higroscópico y poco soluble en agua (su grado de solubilidad es de 9,3 g por 100 ml de agua a 25 ° C), a pesar de ser el fenol más soluble en agua. Es soluble en disolventes orgánicos y soluciones alcalinas. En contacto con la piel produce manchas blancas, y un contacto prolongado permite su penetración en los tejidos más profundos, provocando quemaduras (acción cáustica).
Los fenoles son tóxico, destruye todo tipo de células. Debido a esta acción sobre los microorganismos, tienen acción antiséptica y se utilizan como desinfectantes. Cuando se ingieren, “provocan quemaduras intensas en la boca y garganta, fuertes dolores abdominales, cianosis, debilidad muscular y coma. Se pueden observar temblores y contracciones musculares. La muerte puede resultar de un paro respiratorio «1. Cuando se inhalan, “provocan disnea y tos. La absorción sistémica daña el hígado, los riñones y el sistema nervioso central ”1.
LA toxicidad de los fenoles, particularmente el hidróxido de benceno, se considera de importancia química y pueden surgir problemas incluso cuando esta sustancia entra en contacto con la piel. “Puede causar de todo, desde eritema hasta necrosis y gangrena tisular, dependiendo del tiempo de contacto y la concentración de las soluciones. El mayor peligro del fenol es la capacidad de penetrar rápidamente en la piel, provocando lesiones graves que pueden ser fatales ”.1. Por lo tanto, no se recomienda utilizarlo como desinfectante común, como se hizo recientemente. Su manipulación debe realizarse con los EPI necesarios.
Propiedades fisicoquímicas de los compuestos fenólicos.
En cuanto a las propiedades fisicoquímicas, los compuestos fenólicos presentan un comportamiento similar a los alcoholes, debido a la presencia de hidroxilo. En solución acuosa presentan un carácter ácido, debido a la electronegatividad del átomo de oxígeno del hidroxilo, sin embargo este carácter se considera débil, debido a la resonancia en el anillo aromático. Los monofenoles simples son líquidos o sólidos con puntos de fusión bajos, otros fenoles son sólidos. En relación a la temperatura de ebullición, estos son elevados, debido a su capacidad para formar enlaces de hidrógeno, propiedad que también confiere a los compuestos fenólicos solubilidad en agua. La mayoría de los compuestos son polares, pero hay excepciones, como algunos difenoles, con OH– en las posiciones 1,4 que son no polares. Los compuestos fenólicos son tóxicos e irritantes y tienen un olor fuerte característico.
Hay una serie de compuestos fenólicos, tanto sintéticos como naturales, que están presentes en nuestra vida diaria. Tenemos desde estructuras más simples como el fenol, que está presente en medicamentos y desinfectantes, hasta estructuras más complejas como el estradiol, una hormona sintetizada por el cuerpo femenino, o las tetraciclinas utilizadas en los antibiótico
Curiosidades
- La aspirina (ácido acetilsalicílico) se produce al reaccionar con fenol.
- El THC (tetrahidrocarbinol) es el principio activo presente en la planta de marihuana (cannabis), y por tanto, el fenol es el responsable de sus efectos.