Tabla de contenidos
La hemoglobina (Hb) es una proteína que se encuentra dentro de los eritrocitos o glóbulos rojos.
Su función principal es llevar oxígeno desde los pulmones a todos los tejidos del cuerpo. Al mismo tiempo también lleva parte del dióxido de carbono de los tejidos a los pulmones.
Es la hemoglobina la que da a los glóbulos rojos su color rojo.
Los glóbulos rojos son glóbulos rojos, compuestos de hemoglobinas y globulinas.
Estructura y composición
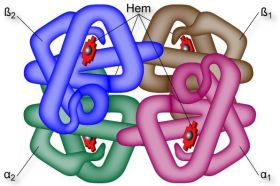
La hemoglobina es una proteína de estructura cuaternaria.
Se compone de cuatro cadenas de globina (parte proteica) es un grupo hemo (grupo protésico) conectado a cada uno de ellos.
En los adultos, las cadenas de globina son de dos tipos: dos de tipo α (alfa) y dos de tipo β (beta).
El grupo hemo contiene un átomo de hierro central en su interior, mantenido en estado ferroso. El hierro es responsable de la absorción de oxígeno, ya que el mineral se une fácilmente al oxígeno.
Estructura de la hemoglobina
La globina no solo cumple la función estructural, sino que también hace posible la reversibilidad del enlace entre el hierro y el oxígeno.
Tipos de hemoglobina
En un sujeto normal, hay tres variantes de hemoglobina (Hb) genéticamente controlada: HbA, HbA2 y HbF (F para fetal). Este último, predominantemente en el feto y el lactante, es reemplazado gradualmente por HbA durante el primer año de vida.
Las cadenas de globina pueden ser de tipos: alfa, beta, gamma, delta, épsilon y zeta. Se producen en diferentes etapas de desarrollo.
Entonces tenemos diferentes hemoglobina diferentes a lo largo de la vida:
- Hemoglobina embrionaria
- hemoglobina fetal
- Hemoglobina en adultos
Las combinaciones entre los diferentes tipos de cadenas dan como resultado diferentes moléculas de hemoglobina.
La hemoglobina anormal más conocida es la HbS – hoz (hoz, en portugués, por su forma), responsable de anemia de células falciformes.
Todavía existe el hemoglobina glucosilada o glucosilada. Corresponde a la unión de la hemoglobina con la glucosa presente en la sangre. Una vez encendida, la glucosa permanece en la hemoglobina durante toda su vida, entre dos y tres meses.
La hemoglobina glicosilada se usa para diagnosticar y controlar la diabetes.
Cuanto más azúcar en la sangre, mayores son las posibilidades de que la hemoglobina esté glicosilada.
Lea también sobre:
Transporte de gas
Como hemos visto, la hemoglobina puede unirse a oxígeno y / o dióxido de carbono.
Transporte de oxígeno (Odos)
- La hemoglobina de los glóbulos rojos que ingresan a los pulmones está ligada al dióxido de carbono;
- En los pulmones, la concentración de oxígeno es mayor que la de dióxido de carbono. Aliado a esto, la hemoglobina tiene afinidad por el oxígeno. Entonces libera dióxido de carbono y se une al oxígeno.
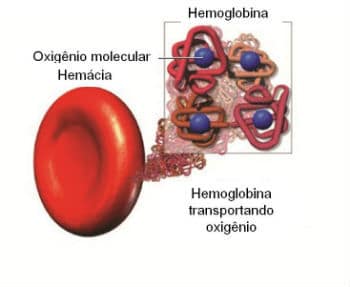
Una molécula de hemoglobina se puede combinar con cuatro moléculas de oxígeno gaseoso. Cuando la hemoglobina se une al oxígeno se llama oxihemoglobina.
Transporte de oxígeno a través de la hemoglobina.
Transporte de dióxido de carbono (COdos)
El transporte de dióxido de carbono es más complejo. Esto se debe a que puede transportarse de tres formas: disuelto en plasma sanguíneo (7%), unido a hemoglobina (23%) y en forma de iones bicarbonato disueltos en plasma (70%).
- La hemoglobina sale del corazón y llega a los músculos a través del torrente sanguíneo;
- Debido al metabolismo, la concentración de dióxido de carbono en el músculo es alta y la concentración de oxígeno es baja;
- Luego, la hemoglobina se une al dióxido de carbono y libera oxígeno.
En esta reacción, el carbaminohemoglobina.
Durante el ejercicio, el músculo produce ácidos (iones de hidrógeno y ácido láctico) que reducen el pH de lo normal.
O pH ácido disminuye la atracción entre el oxígeno y la hemoglobina, lo que hace que se libere más oxígeno de lo normal. Esta condición aumenta la oxigenación de los músculos.
Transporte de monóxido de carbono (CO)
La hemoglobina tiene una alta afinidad por el monóxido de carbono (CO). Cuando la hemoglobina se une al monóxido de carbono se llama carboxihemoglobina.
La afinidad por el monóxido de carbono es hasta 23 veces mayor que la del oxígeno. Sin embargo, esta asociación puede ser letal, el monóxido de carbono impide el transporte de oxígeno a los tejidos del cuerpo.
Obtenga más información sobre los glóbulos rojos.
Función
Oxihemoglobina
Son los hemas de la hemoglobina los que fijan el oxígeno. Cuando la sangre llega a los pulmones, cada uno de los cuatro átomos de hierro de las moléculas de hemoglobina se une con una molécula de oxígeno; así es como el oxígeno se transporta a otros tejidos del cuerpo, donde se libera y se difunde al líquido intersticial.
Cada gramo de hemoglobina transporta 1,34 ml de oxígeno. El grado de saturación está relacionado con la presión de oxígeno, que es igual a 100 mm Hg (milímetros de mercurio) en sangre arterial y 35 mm Hg en sangre venosa.
La afinidad de la hemoglobina por el oxígeno depende del nivel de 2,3-difosfoglicerato (DPG), cuyas modificaciones, por tanto, juegan un papel importante en la adaptación a la hipoxia (ligera disminución de la cantidad de oxígeno distribuido a los tejidos).
Carbhemoglobina
Es en las globinas donde se fija el dióxido de carbono. A nivel de los tejidos, cuando los hemes han liberado oxígeno, cada cadena de proteínas se une con una molécula de dióxido de carbono (desperdicio del metabolismo celular liberado en el líquido intersticial). El torrente sanguíneo conduce la carbhemoglobina a los pulmones, donde se libera y exhala dióxido de carbono.
Enfermedades y hemoglobina
Las anomalías genéticas en la síntesis de cadenas polipeptídicas (p. Ej., Sustitución de un aminoácido por otro o mutación puntual) conducen a enfermedades de la sangre, como la anemia de células falciformes, caracterizada por glóbulos rojos en forma de hoz. La distribución anormal de cadenas polipeptídicas de composición normal conduce a enfermedades de la hemoglobina conocidas como talasemias.
Varias enfermedades, llamadas hemoglobinopatías, se caracterizan por una anomalía en la síntesis de hemoglobina, que consiste en una producción insuficiente o un defecto estructural de la molécula sintetizada. La hemoglobina también puede verse afectada por un cambio accidental (adquirido) en la estructura que reduce su capacidad para transportar oxígeno.
Metahemoglobina es una molécula de hemoglobina modificada por la conversión de hierro ferroso en hemo a hierro férrico, una reacción adversa a un fármaco (dapsona) o debido a una intoxicación por nitritos.
Sulfhemoglobina se debe a la unión del azufre a una molécula de hemoglobina por intoxicación (sulfuro de hidrógeno, sulfonamidas).
Carboxihemoglobina se debe a la unión del monóxido de carbono a una molécula de hemoglobina durante el envenenamiento por este gas.
Estas patologías adquiridas, de muy variable gravedad, solo pueden derivar en cianosis o, además, poner en riesgo la vida del paciente.
Los niveles de hemoglobina se pueden detectar mediante análisis de sangre.
Los valores de referencia para la hemoglobina son:
- Niños de 2 a 6 años: 11,5 a 13,5 g / dl;
- Niños de 6 a 12 años: 11,5 a 15,5 g / dl;
- Hombres: 14 a 18 g / dl;
- Mujeres: 12 a 16 g / dL;
- embarazada: 11 g / dL.
Las diferencias en estos valores pueden indicar problemas de salud:
hemoglobina baja
- Anemia
- Linfoma
- hipotiroidismo
- Sangrado
- Insuficiencia renal
hemoglobina alta
- Deshidración
- Enfisema pulmonar
- tumor de riñón
La hemoglobina en la orina (hemoglobinuria) se detecta mediante un examen. Esta condición puede estar relacionada con problemas renales como infecciones, pielonefritis o cáncer.

![Molécula de hemoglobina y un grupo hemo. Ilustración: OpenStax College [CC-BY-SA 3.0] / vía CNX.org](https://definicionesyconceptos.com/wp-content/uploads/2021/04/Hemoglobina-Biologia-Informacion-escolar.jpg)