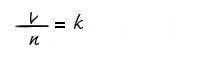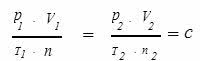Tabla de contenidos
Ley de Avogadro, también conocida como Constante de Avogadro, es un principio establecido en 1811 por el químico italiano Amedeo Avogadro (1776-1856).
Indica que «volúmenes iguales de dos gases cualesquiera bajo las mismas condiciones de presión y temperatura contienen el mismo número de moles de moléculas de gas». Está representado por el símbolo NLA (o L).
El número de Avogadro es 6.022 x 1023 mol-1 y la indicación matemática de la Ley de Avogadro es la siguiente:
- V es el volumen del gas
- norte es la cantidad de sustancias en el gas
- k es una constante de proporcionalidad.
El número de Avogadro es un número estándar para representar un mol de cualquier entidad elemental de átomos, moléculas, iones y electrones. La consecuencia más importante de la ley de Avogadro es la constante del gas ideal y tiene el mismo valor para todos los gases.
Por lo tanto, la Constante de Avogadro se señala la siguiente forma:
Dónde:
- PAG es la presión del gas
- t es la temperatura del gas
- C es la constante
El número de Avogadro tiene el mismo valor para todos los gases, independientemente del tamaño o la masa de las moléculas de gas.
Para obtener más información, lea también:
Ejercicios resueltos
Ejemplo 1: ¿Cómo calcular la masa de un átomo de carbono (C)?
Paso 1: busque la masa atómica de carbono en la tabla periódica
La masa atómica del elemento químico carbono es = 12.01 u
1 mol de carbono es igual a 6,002 x 1023 (El número de Avogadro)
Paso 2: convierte un átomo de carbono en gramos
Masa de C = 12.01 g / 6.022 x 1023 Átomos de C
Respuesta:
Masa de C = 1.9994 x 10-23 gramo
Ejemplo 2: Cuántas moléculas de Hdos0 ¿hay en un copo de nieve que pesa 1 mg?
Paso 1: Determine la masa de 1 mol de Hdos0
Cómo se hacen los copos de nieve de Hdos0, para obtener la masa de 1 molécula de agua, es necesario determinar las masas atómicas de hidrógeno y oxígeno. Esto se hace a partir de la tabla periódica.
Hay dos átomos de hidrógeno y uno de oxígeno por cada molécula de HdosO, de modo que la masa de HdosO es:
masa de H 2 O 2 = (masa de H) + masa de O
masa de H 2 O = 2 (1.01 g) + 16.00 g
masa de HdosO = 2,02 g + 16,00 g
masa de HdosO = 18,02 g
Paso 2: Determine la cantidad de moléculas de HdosO en un gramo de agua
Un mol de HdosO es igual a 6.022 x 1023 Moléculas de HdosO (número de Avogadro). Esta relación se utiliza para convertir varias moléculas de HdosLos gramos por proporción:
masa de X moléculas de HdosMoléculas O / X = masa de un mol de Hdos0 moléculas / 6.022 x 1023 moléculas
Cálculo para X moléculas de HdosO:
Moléculas X HdosO = (6.022 x 1023 Moléculas de HdosO) / (masa de un mol de HdosO · masa de X moléculas de HdosO
Así:
Moléculas X HdosO = (6.022 x 1023 Moléculas de HdosO) / (18,02 g · 1 g)
Moléculas X HdosO = 3,35 x 1022 moléculas / gramo
Hay 3,35 x 1022 Moléculas de HdosO en 1 g de HdosO.
Nuestro copo pesa 1 mg y 1 g = 1.000 mg.
Moléculas X HdosO = 3,35 x 1022 moléculas / gramo · (1 g / 1000 mg)
Respuesta:
Hay 3,35 x 1019 Moléculas de HdosO en 1 mg de un copo de nieve.