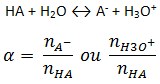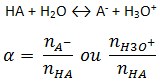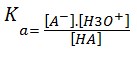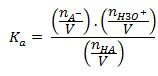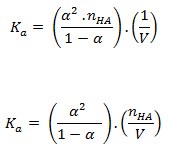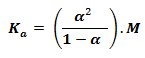El grado de ionización de un ácido indica el porcentaje o fracción molar de iones H3O+ formado por la liberación de iones H+ de un ácido de Arrhenius o anión correspondiente en relación con la cantidad inicialmente añadida. Así, si 1 mol de ácido monoprótico HA se diluye en agua líquida pura y, de esta cantidad de materia, 0,05 mol está completamente ionizado, se puede decir que el grado de ionización será del 5% o α = 0,05. Por tanto, el 95% del ácido (0,95 mol) permanecerá en forma molecular:
La constante de ionización de un ácido tiene en cuenta la concentración de las especies involucradas y no solo la cantidad de materia. Para esta reacción:
Es de destacar que la concentración de HdosO ya está incorporado al valor de Klos, el cual, por ser un solvente cuya concentración es extremadamente alta (incluso porque las concentraciones de H3O+ y oh– son del orden de 10-7 M) no es parte del denominador de la ecuación constante.
Otro punto a destacar es que la concentración de HA no será la misma que la inicial, ya que una parte de ella sufrió ionización. Por lo tanto, el número de moles de iones de aniones o hidroxones debe «descontarse» del total.
LOS Ley de dilución de Ostwald se describe con precisión como la relación matemática entre el grado de ionización α (en fracción molar) y la constante de equilibrio Klos.
De la definición de concentración proviene:
Aplicando en la fórmula de Klos:
De la definición de grado de ionización proviene:
Considerando el «descuento» en el número de moles de HA (inicialmente igual anHAY y ahora como nHAY – α. noHAY) y sustituyendo en la fórmula de Klos:
Y, como nHAY/ V = concentración inicial M del ácido, finalmente:
Si el ácido tiene un grado de ionización muy pequeño, el valor 1-α se puede aproximar a 1, así:
Es importante recordar que esta relación solo se puede utilizar en reacciones de ionización de ácido monoprótico (con un átomo de hidrógeno ionizable) o poliprótico considerando solo una ionización a la vez (ya que los valores de α y M cambiarán con cada disociación).