Tabla de contenidos
El litio es un elemento químico de símbolo Li, número atómico 3, masa atómica 7, perteneciente al grupo 1 (Familia 1A), siendo un metal alcalino. Su nombre deriva del griego Lithos, que significa piedra, ya que el elemento se encuentra en las rocas.
Es metal alcalino, el más ligero de todos los metales. (Elemento del símbolo Li.)
- Número atómico: 3
- Masa atomica : 6.941
- Temperatura de fusión : 180,54°C
- Densidad : 0,53 g/cm23
Propiedades químicas
El litio fue descubierto en 1817 por el sueco Johann August Arfvedson (1792-1841), quien logró extraer su hidróxido, la litina, de su principal mineral, la lepidolita. Más tarde fue aislado por electrólisis por Sir H. Davy. Es el primero de los metales alcalinos en la tabla periódica de elementos y el metal sólido más ligero. La química del litio es esencialmente iónica: al combinarse con elementos electronegativos, forma sólidos iónicos cristalizados, solubles en agua. Reacciona con oxígeno, hidrógeno, nitrógeno y agua. Se encuentra en la naturaleza en forma de silicatos y fosfatos.
Producción
Los principales países productores de litio, en forma de carbonato, son Argentina, Chile, China y Estados Unidos. Otros compuestos y concentrados son suministrados principalmente por Australia, Brasil, Canadá, Portugal, Rusia y Zimbabue. Las mayores reservas se encuentran en los desiertos y lagos salados, particularmente en Bolivia (desierto de Uyuni) y China, Qinhai y Tíbet.
Usos en la industria
En la industria química, el litio se utiliza como agente complejante para la síntesis de compuestos orgánicos. En la industria aeronáutica, participa en la producción de aleaciones ligeras de altas prestaciones (especialmente aluminio-litio).
Su gran potencial electroquímico también hace que el litio se pueda utilizar como electrodo para la fabricación de baterías y acumuladores. A partir de finales de la década de 1970 se iniciaron investigaciones con el fin de encontrar pares electroquímicos con mejores prestaciones que los acumuladores de plomo o de níquel-cadmio utilizados hasta entonces. Condujeron a la aparición de una primera generación de baterías de litio, denominadas metal de litio, que comprende un electrodo negativo a base de litio metálico. Sin embargo, esta tecnología se ha topado con problemas relacionados con la mala reconstitución del electrodo negativo de litio durante las sucesivas cargas. Estas dificultades se han superado con el desarrollo de baterías iones de litio, presenta un nuevo tipo de electrodo negativo a base de carbono, utilizado como compuesto de inserción de litio. Comercializados desde 1991, ahora equipan muchos dispositivos electrónicos portátiles (ordenadores, videocámaras, cámaras, walkmans, teléfonos móviles, etc.). La industria automotriz tiene grandes esperanzas en el futuro uso de baterías de litio para impulsar vehículos eléctricos o híbridos; ya se han probado prototipos y se continúa investigando activamente para desarrollar dispositivos menos costosos y más eficientes (autonomía, seguridad, etc.) que los disponibles en la actualidad.
Sin embargo, los recursos mundiales de litio son extremadamente limitados (se estiman en 4 millones de toneladas) y parece difícil prever, además del crecimiento del mercado ya observado para equipos electrónicos, una producción masiva de baterías de litio para automóviles.
Uso de sales de litio en psiquiatría
Las sales de litio utilizadas en el tratamiento de los trastornos psíquicos son el gluconato y el carbonato de litio. Estos son psicotrópicos (sustancias activas en la psique) reguladores del estado de ánimo (timorreguladores).
Están indicados en una enfermedad psiquiátrica, enfermedad maníaco-depresiva (o enfermedad bipolar), caracterizada por episodios alternos de depresión y excitación eufórica. Se administran por vía oral.
El tratamiento tiene una duración de varios años y requiere una estrecha vigilancia del estado físico del paciente. Además, se prescriben análisis de sangre periódicos para comprobar que la concentración de litio en sangre (litemia) permanece en la zona terapéutica.
Las sales de litio están contraindicadas en caso de insuficiencia renal y formalmente en caso de embarazo. No se recomienda la combinación con diuréticos, antiinflamatorios no esteroideos y antidepresivos, ya que puede aumentar la litemia. Hay muchos efectos secundarios. Están representados principalmente por náuseas, temblores, trastornos del equilibrio, sensación de sed y riesgos de tiroides y riñones.
Características
[ width=»600″]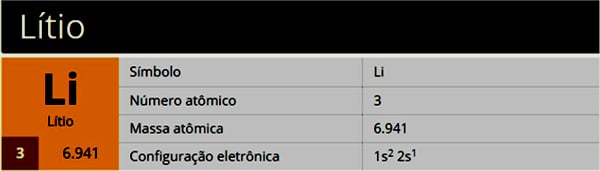
Debido a que es un elemento muy reactivo, no se encuentra aislado en la naturaleza. En su forma pura se oxida fácilmente en presencia de aire o agua.
Se encuentra en los minerales espodumenio, lepidolita y petalita. Además de las rocas, también se da en aguas saladas y termales. En entornos industriales, se obtiene mediante la electrólisis de cloruro de litio.
Se caracteriza por ser un metal blando, blando y de color plateado. En contacto con el aire adquiere color gris, por lo que es común conservarlo en aceite mineral.
Entre sus otras características se encuentran:
- Buen conductor de electricidad;
- Extremadamente reactivo;
- Muy inflamable;
- El metal de menor densidad es incluso menos denso que el agua.
Obtenga más información, lea también:
aplicaciones
El litio tiene varios tipos de uso, desde aplicaciones industriales hasta la producción de medicamentos:
- Fabricación de baterías a partir de iones de litio;
- Participa en el funcionamiento de marcapasos cardíacos;
- El carbonato de litio se utiliza en la formulación de fármacos psiquiátricos, como contra la depresión bipolar y tranquilizantes;
- Participa en la formación de aleaciones metálicas;
- Producción de lubricantes para máquinas que trabajan a altas temperaturas;
- Fabricación de cerámica y vidrio resistentes al calor;
- Sistemas de secado industrial en forma de cloruro o bromuro de litio.