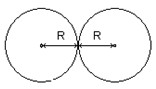
O rayo atómico es una de las propiedades periódicas de los elementos químicos y representa la distancia entre el centro del núcleo de un átomo y la capa más externa de la electrosfera (capa de valencia). Se calcula a partir de una molécula diatómica del mismo elemento a la mitad de la distancia entre los respectivos núcleos. Porque, como el átomo no es una esfera, el cálculo del radio cuando está aislado es demasiado impreciso.

El radio atómico también está intrínsecamente ligado a la propiedad periódica de la electronegatividad. Cuanto mayor es esta propiedad, mayor es la fuerza que atrae el núcleo a la electrosfera y menor el radio.
De manera similar, cuanto mayor es el radio atómico, menor es el potencial de ionización, ya que la electrosfera no es tan fuertemente atraída por el núcleo y el electrón de valencia se puede eliminar más fácilmente; y menor afinidad electrónica, porque, con menos fuerza de atracción en la electrosfera, se libera una menor cantidad de energía al recibir un electrón.
Fuentes:
http://www.crystalmaker.com/support/tutorials/crystalmaker/atomicradii/
http://pt.wikipedia.org/wiki/Atomic_Ray