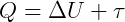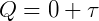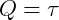Existe una comparación didáctica entre las tres leyes de la termodinámica:
- 1ª Ley: no se puede ganar;
- 2ª Ley: ni siquiera puedes dibujar;
- 3ª Ley: solo se puede empatar al cero absoluto.
En otras palabras, la primera ley define que la energía solo se transforma de una forma a otra y no puede crearla, de ahí la expresión «no se puede ganar». La segunda ley establece que además de no poder ganar (crear energía), una parte todavía se pierde, ya que no es posible transformarlo todo en trabajo, de ahí la expresión «o incluso romper».
ya el tercera ley de la termodinámica establece que en el cero absoluto es posible que una máquina tenga una eficiencia del 100%, es decir, la energía térmica, en forma de calor, se puede transformar totalmente en trabajo, sin pérdidas. Por eso se dijo que en el cero absoluto puede haber un «empate», ya que la energía no se crea, pero tampoco se pierde, ya que se transforma en su totalidad.
En el cero absoluto, la energía interna del cuerpo es cero, sin movimiento molecular. Según la primera ley de la termodinámica:
como ΔU = 0,
el calor se convertiría totalmente en trabajo.
Sin embargo, el cero absoluto nunca se alcanzó en el laboratorio, lo que hace que la hipótesis de la tercera ley solo sea teórica cuando la temperatura es exactamente igual a cero. Sin embargo, las hipótesis para situaciones en las que el la temperatura se acerca al cero absoluto.
En 1907, Walther Nernst (1864-1941) propuso una ley que se ocupaba de estas situaciones, en las que la temperatura se acerca al cero absoluto:
«La entropía del sistema tiende a cero si su temperatura tiende a cero.«
Esta ley de Nernst se conoció como la Tercera ley de la termodinámica.
Max Planck (1858-1947) también llegó a resultados idénticos, sin embargo, considera la entropía nula, en el cero absoluto, solo para sustancias puras, no para mezclas.
LOS entropía mide el nivel de desorganización molecular en el sistema. Cuanto mayor es la temperatura, mayor es la entropía, ya que las moléculas más calientes se mueven más y tienden a extenderse a través del volumen. Con el concepto de entropía, la Segunda Ley de la Termodinámica también se puede escribir de la siguiente manera:
«Si un proceso tiene lugar en un sistema cerrado, la entropía nunca disminuye, permaneciendo constante para procesos reversibles o aumentando para procesos irreversibles.«
Demanda judicial reversible pueden volver a su estado inicial, mientras que el irreversible no. Un ejemplo práctico es cuando se coloca una gota de agua en una placa calefactora para que se caliente. La gota difícilmente volverá a su estado inicial y este proceso es irreversible. Por otro lado, un recipiente con agua, al enfriarse, se convierte en un volumen de hielo, pero si se calienta, puede volverse líquido nuevamente, siendo un proceso reversible.
En el contexto de las tres leyes, es imposible tener una máquina térmica con 100% de eficiencia, se considera un proceso reversible el proceso ideal mediante el cual se obtiene la máxima eficiencia en una máquina térmica, incluso si todavía tiene η <1.
Se destacan algunos factores que hacen que un proceso sea irreversible, como reacciones químicas espontáneas, fricción en deslizamientos o flujo de fluido, expansión de gases o líquidos a una presión menor sin resistencia, deformación inelástica, flujo de corriente eléctrica en resistencias, transferencias de calor en sistemas con finito diferencia de temperatura, entre otros.