La transformación isobárica corresponde a los cambios que se producen en los gases a presión constante.
Cuando una masa de gas cambia de estado cuando la presión no cambia, el volumen y la temperatura del gas varían.
La ley que gobierna esta transformación es la Ley de Charles y Gay-Lussac. Los científicos Jacques Alexandre Charles y Joseph Louis Gay-Lussac, a través de sus experimentos, llegaron a la conclusión de que:
«Si la presión de una masa de gas es constante, entonces la relación entre volumen y temperatura también es constante».
¿Cómo ocurre la transformación isobárica?
El prefijo Yo asi indica que la grandeza es constante. Por tanto, en el proceso isobárico la presión se mantiene constante al realizar una transformación.
Esto significa que si un gas sufre sucesivos cambios a presión constante, el cociente entre volumen y temperatura es el mismo.
Fórmula de transformación isobárica
Matemáticamente, en cualquier estado, la transformación isobárica se expresa mediante la fórmula:
Dónde,
V: volumen ocupado por el gas;
T: temperatura absoluta del gas;
K: constante de presión, que relaciona la masa, la presión y la naturaleza del gas.
Otra forma de interpretar la relación entre las magnitudes de la Ley de Charles y Gay-Lussac es decir que una masa de gas sometida a una transformación a presión constante tiene una variación de volumen directamente proporcional a la variación de temperatura.
Por tanto, la variación se produce de manera uniforme: si duplicamos una cantidad, la otra aumenta en la misma proporción. Asimismo, si lo cortamos por la mitad, el otro también disminuye.
En una expansión isobárica hay un aumento en el volumen de gas, ya en el compresión isobárica hay una disminución en el volumen del gas.
Gráficos de transformación isobárica
Al relacionar las variables de volumen y temperatura, el gráfico se presenta como un segmento de línea.
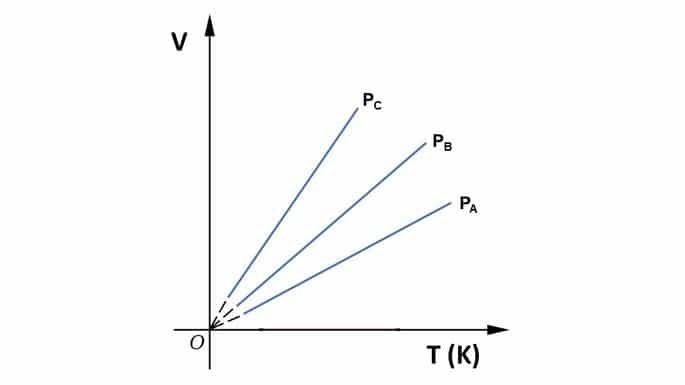
Si usamos el diagrama para comparar tres presiones diferentes del mismo gas, donde pa> pb> pc, la constante en la relación es inversamente proporcional a la presión y, por lo tanto, ka A través del gráfico con las cantidades volumen y presión es posible calcular el trabajo en la transformación isobárica. El área de la figura corresponde al trabajo, que se puede calcular mediante: Dónde, W: trabajo; Obtenga más información sobre las transformaciones de gas. En una transformación isobárica, un gas que llena un recipiente de 3,0 l está inicialmente a una temperatura de 450 K. El estado final del gas indica que su temperatura ha disminuido a 300 K. ¿Cuál es el volumen del gas al final de la ¿transformación? a) 1,0 l Un gas ha sufrido una transformación a presión constante y, como resultado, su volumen ha aumentado en un 80%. Sabiendo que en el estado inicial la masa de gas estaba en el CNTP (condiciones normales de temperatura y presión), determinar la temperatura del gas, en grados Celsius, luego de este proceso. Datos: a) 198,6 ºC Continúe sus estudios leyendo también sobre: ÇENGEL, YA; BOLES, MA Termodinámica. 7ª ed. Porto Alegre: AMGH, 2013. HELOU; GUALTER; NEWTON. Temas de física, vol. 2. São Paulo: Editora Saraiva, 2007. 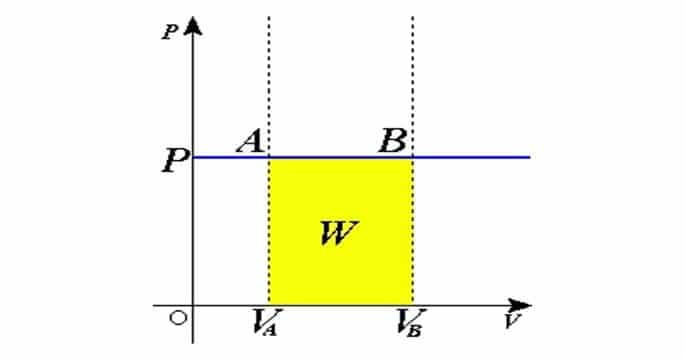
p: presión constante;: variación de volumen.
Ejercicios sobre transformaciones isobáricas
Pregunta 1
b) 2,0 l
c) 3,0 l
d) 4,0 lPregunta 2
b) 186,4 ºC
c) 228,6 ºC
d) 218,4 ºCReferencias bibliográficas