La materia puede presentarse en diferentes estados físicos. Son ellos:
- Sólido: forma adecuada y volumen bien definido, las moléculas que componen el cuerpo vibran alrededor de una posición fija;
- Líquido: sin forma propia, toma la forma del recipiente en el que está contenido, pero con su volumen todavía bien definido. Las moléculas ya no vibran en una posición fija, sino que siguen unidas entre sí, yendo de un lugar a otro;
- Gaseoso: ni forma ni volumen definidos, asumiendo los del recipiente en el que se encuentra, con las moléculas ya no unidas entre sí, yendo en cualquier dirección en el volumen en el que se encuentra.
Dependiendo de factores, como la temperatura y la presión, la materia puede sufrir un cambio de estado, que sería la alternancia entre los estados sólido, líquido y gaseoso. Consulte la figura 1, a continuación, para ver los nombres de estos cambios.
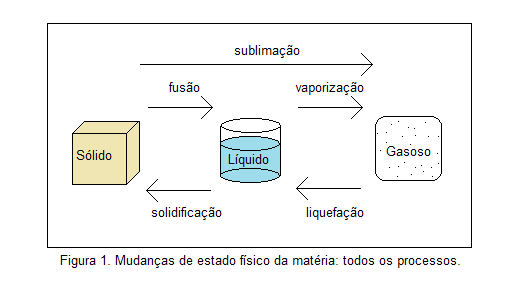
Aquí estudiaremos con más profundidad el cambio de estado denominado vaporización. Se caracteriza por el cambio de estado líquido a gaseoso y esto puede ocurrir de tres formas: hirviendo, evaporación y calefacción. Veamos las características de cada uno a continuación.
En este proceso, la transición del estado líquido al gaseoso ocurre en toda la masa líquida. Esto sucede cuando la presión de vapor del líquido es igual a la presión externa y este vapor comienza a escapar a la atmósfera. Para que el líquido hierva, debe alcanzar una cierta temperatura, la temperatura de ebullición, que es un valor característico de cada líquido.
A presión normal, al nivel del mar, la temperatura del agua hirviendo es de 100ºC, por ejemplo. Cuanto mayor sea la altitud de la ubicación, menor será la presión y menor la temperatura de ebullición. En el Everest, la montaña más alta de la Tierra, cuyo pico tiene 8.848 m de altura en relación al nivel del mar, la temperatura de ebullición del agua es de 75º C.
La transición del estado líquido al gaseoso, en la evaporación, ocurre lentamente y solo en la superficie del líquido. Un líquido, a cualquier temperatura, tiene partículas que tienen una energía cinética promedio, algunas más rápidas, otras más lentas. Debido a las colisiones intermoleculares entre ellos, los que eran lentos pueden volverse rápidos y viceversa. Ante la ocurrencia de este fenómeno, las partículas que se encuentran en la superficie son bombardeadas por las partículas que se encuentran debajo, ganando una gran cantidad de energía cinética, hasta el punto de que algunas de ellas salen del líquido hacia la atmósfera, convirtiéndose en moléculas de vapor.
Al desprenderse del líquido, las moléculas que tenían alta energía cinética al salir, tienden a disminuir esta energía. Esto se debe a una atracción que existe entre ellos y los que permanecen en el líquido. Por tanto, estas moléculas de vapor que están justo encima del líquido tienen poca energía y provocan un enfriamiento inmediatamente por encima del líquido. Este efecto refrescante se nota con el alcohol ordinario, que se evapora rápidamente y, al pasar sobre la piel, inmediatamente sentimos el enfriamiento.
Gracias a las glándulas sudoríparas del cuerpo humano, que producen la transpiración, el proceso de evaporación del sudor hace que el cuerpo se enfríe, equilibrando su temperatura. Algunos animales no tienen estas glándulas sudoríparas y necesitan estar en lugares de menor temperatura para refrescarse, como los cerdos, que están en el barro. Otros animales utilizan otros recursos, como los perros, que lo hacen respirando, evaporándose por la boca y dentro del tubo bronquial.
No existe una temperatura específica del líquido para que se produzca la evaporación, como en el caso de la ebullición. Es por eso que cuando dejamos la ropa en el tendedero o un lavabo con agua (o cualquier otro líquido) al aire libre, la evaporación se produce de forma gradual y constante. Pero sabemos que cuanto mayor es la temperatura del líquido, más rápida es la evaporación. Otros factores que ayudan a acelerar la evaporación son:
- el tipo de líquido (algunos tienen más probabilidades de evaporarse que otros: volatilidad);
- la presión ejercida sobre el líquido, porque cuanto más pequeño es, más rápido será el proceso; y
- la superficie de contacto expuesta al medio ambiente, y debe ser lo más grande posible.
En este proceso, el líquido se somete a una rápida transmisión de calor, de manera que la superficie del líquido alcanza el punto de ebullición antes de que su interior se caliente, ocurriendo inmediatamente la vaporización en la superficie del líquido. La superficie que transmite calor al líquido debe tener una temperatura superior al punto de ebullición del líquido en contacto. Esto es lo que sucede cuando rocía gotas de agua en un plato caliente, por ejemplo.
Evaporación
La evaporación es un proceso de vaporización en el que el cambio de estado se produce de forma gradual.
Las partículas dentro de un líquido tienen velocidades variables. Así, hay partículas con valores de energía cinética más altos que otras.
Estas partículas escapan cuando tienen una velocidad suficientemente alta a través de la superficie libre del líquido.
De esta forma, dejan de sufrir la acción de las fuerzas internas de unión del líquido y pasan al estado gaseoso.
Hay algunos factores que influyen en la velocidad a la que se produce la evaporación. Podemos mencionar: temperatura, naturaleza y área de la superficie libre del líquido, presión y concentración de vapor cerca de la superficie libre del líquido.

Hirviendo
Cuando un cuerpo recibe calor aumenta el grado de agitación entre las partículas que lo componen y consecuentemente también aumenta su temperatura.
Al alcanzar un cierto valor de temperatura, llamado punto de ebullición, la sustancia comenzará a cambiar de fase.
Por ejemplo, el agua, a presión de 1 atmósfera, comienza a hervir cuando alcanza una temperatura de 100 ºC. El hierro, en cambio, solo hervirá cuando su temperatura sea igual a 2 800 ºC.
La ebullición es un proceso de vaporización más rápido que la evaporación y la temperatura durante la ebullición permanece constante.
Además, para que un líquido se convierta completamente en gas, necesita recibir una cierta cantidad de calor.
El calor latente de ebullición es la cantidad de calor por unidad de masa que debe recibir un cuerpo para pasar a la fase gaseosa. Este valor depende de la sustancia que lo constituye.

Calefacción
El calentamiento es un tipo de vaporización que se produce cuando se libera un líquido sobre una superficie que tiene una temperatura superior a la de su punto de ebullición.
En esta situación, el líquido cambiará rápidamente a un estado gaseoso.
Un ejemplo de calentamiento es cuando echamos unas gotas de agua en un plato muy caliente.
Cambios de fase
Además de la vaporización, existen otros procesos de cambio de estado. Son ellos:
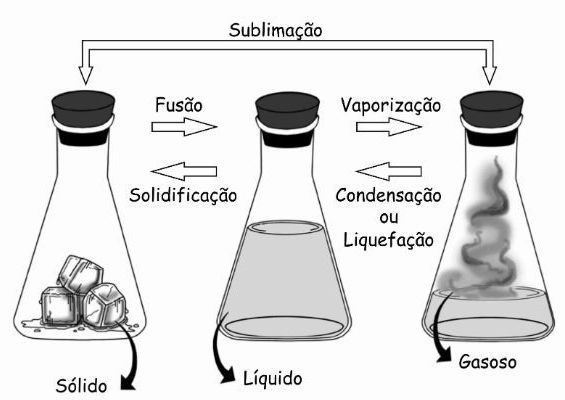
Conocer más sobre: