La molécula es un grupo estable de dos o más átomos, iguales o diferentes, unidos mediante enlaces covalentes.
Los compuestos moleculares se clasifican según su polaridad.
- Moléculas apolares: no hay diferencia de electronegatividad entre los átomos.
- Moléculas polares: hay una diferencia de electronegatividad entre los átomos, con un polo positivo y un polo negativo.
Cuando la molécula está formada por más de un elemento químico, el número de nubes electrónicas y ligandos del átomo central determina la polaridad.
Moléculas no polares
Las moléculas tienen sus átomos unidos por enlaces covalentes, es decir, se comparten electrones.
La electronegatividad es la capacidad de un átomo de atraer electrones a un enlace, formando polos en la molécula.
El átomo que atrae los electrones se convierte en el polo negativo, debido a la acumulación de carga negativa, y el otro átomo se convierte en el polo positivo.
Cuando una molécula está formada por átomos de un solo elemento químico, no hay diferencia en la electronegatividad y la molécula es apolar.

Moléculas de sustancias simples, como Odos y Ndos, están formados por átomos del mismo elemento; las moléculas de sustancias compuestas tienen al menos dos elementos diferentes.
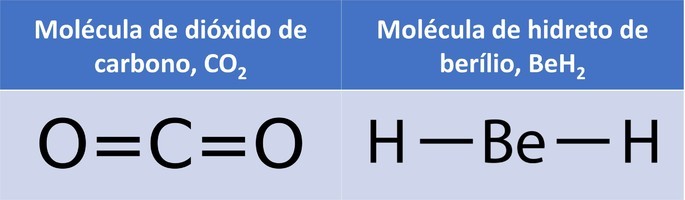
Moléculas de COdos y BeHdos también son apolares debido a la geometría. Como ambos tienen geometría lineal, los átomos de las extremidades, oxígeno e hidrógeno, atraen los electrones del enlace entre sí, ya que son más electronegativos.
La atracción del átomo de la izquierda se compensa con la atracción del átomo de la derecha. Dado que los enlaces son los mismos, es decir, tienen la misma intensidad, pero diferentes direcciones, las moléculas no forman polos.
Moléculas polares
Cuando una molécula está formada por diferentes átomos, existe una diferencia en la electronegatividad, pero es la geometría de la molécula la que determina si será polar o no polar.

En los dos ejemplos, vemos que los átomos centrales, oxígeno y nitrógeno, tienen pares de electrones desapareados que forman nubes electrónicas.
Dado que hay más nubes electrónicas alrededor del átomo central que átomos iguales unidos a él, la molécula es polar.
Con la formación de una nube electrónica, la molécula asume una estructura que se adapta mejor a los átomos y, por tanto, la geometría del agua es angular y la del amoniaco piramidal.
¿Quieres enriquecer tus conocimientos? ¡No te pierdas los textos a continuación!
Ejercicio con comentarios comentados
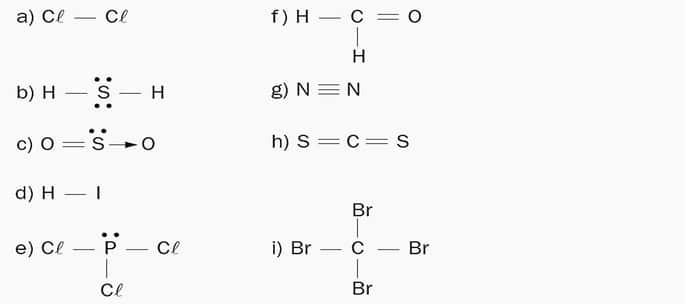
1. Indique la polaridad de las moléculas:
dos. (Fuvest) Considere las moléculas de HF, HCl, HdosOHdos, Odos y CH4.
a) Clasifica estas moléculas en dos grupos: polares y apolares.
b) ¿Cuál es la propiedad referente al átomo y cuál se refiere a la molécula en la que se basó para clasificarlos?
3. (Vunesp) Entre las alternativas a continuación, indique la que contiene la declaración incorrecta:
a) Enlace covalente es el que se produce al compartir electrones entre dos átomos.
b) El compuesto covalente HCl es polar, debido a la diferencia de electronegatividad entre los átomos de hidrógeno y cloro.
c) El compuesto formado entre un metal alcalino y un halógeno es covalente.
d) La sustancia de fórmula Brdos es apolar.
e) La sustancia de fórmula Caldos es iónico.
Asegúrese de consultar estos textos sobre temas relacionados con el tema de este contenido: