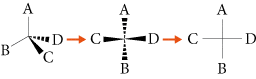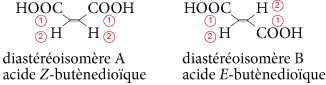Tabla de contenidos

Campo de la química que estudia la estructura espacial de las moléculas, así como sus consecuencias sobre sus propiedades fisicoquímicas.
«Estereoquímica es sinónimo de química en el espacio». Esta definición es la dada por los químicos Joseph Le Bel y Jacobus Van’t Hoff en 1874. Sin embargo, esta definición sería errónea si como consecuencia consagrara la existencia de dos químicas, una de las cuales sería espacial. Las reacciones químicas, que implican acercarse a los reactivos y establecer un estado de transición, siempre tienen lugar en un espacio tridimensional. Además, las moléculas cuya estructura estamos examinando no están completamente definidas por una fórmula plana; Por tanto, es fundamental especificar la posición relativa de los átomos entre sí.
De hecho, la estereoquímica y la química son inseparables. De hecho, la química bidimensional solo implica fórmulas crudas o fórmulas planas desarrolladas (o semielaboradas) y resulta totalmente insuficiente en cuanto se examina en detalle un fenómeno químico (mecanismo de reacción, por ejemplo). Los modelos moleculares y su representación simbólica plana son de gran ayuda para el químico, que puede predecir isomerías (diferentes disposiciones de los átomos de una molécula a partir de una fórmula cruda) e interpretar reacciones. Por lo tanto, la estereoquímica enfatiza el aspecto estérico de la química, y se obtiene información valiosa al examinar una reacción, por simple que sea, en términos de su estereoquímica.
1. Historia de la estereoquímica

Fue el físico francés Jean-Baptiste Biot quien abrió el camino a la estereoquímica en 1815 al descubrir la actividad óptica, propiedad que tienen ciertas sustancias orgánicas de modificar la polarización de la luz. Luego, en 1848, Louis Pasteur utilizó este principio y logró separar dos variedades cristalinas, imagen una de la otra en un espejo: tartrato doble de sodio y amonio (formado a partir del ácido tartárico racémico). Esta primera división espontánea de un llamado compuesto racémico (mezcla 50/50 de cada uno de los dos enantiómeros, imagen de uno del otro en un espejo plano pero no superponible) destaca una isomería particularmente importante, la isomería óptica. Por tanto, la estereoquímica jugará un papel fundamental en el desarrollo de la química.
Treinta años después, Joseph Le Bel y Jacobus Van’t Hoff se basan principalmente en la isomería óptica de los compuestos para establecer la estructura tetraédrica del carbono. De hecho, el centro de asimetría del átomo de carbono imprime una rotación inversa en la luz polarizada en cada enantiómero.
La disposición de los enlaces alrededor de un átomo de nitrógeno también se estudia mediante métodos estereoquímicos. Se muestra que el amonio cuaternario y los óxidos de nitrógeno pueden ser ópticamente activos. Por tanto, el nitrógeno de estos compuestos no tiene una estructura plana. Los compuestos de azufre, fósforo, arsénico … también son examinados por estas técnicas
La química de los complejos metálicos progresó considerablemente siguiendo el trabajo de Alfred Werner, quien ganó el Premio Nobel de Química en 1913. Werner planteó la revolucionaria hipótesis de que el cobalto o el níquel son octaédricos en complejos donde estos metales están hexacoordinados. El átomo metálico está en el centro de un octaedro y las coordenadas están dispuestas en los vértices. Esta representación de los enlaces químicos alrededor del metal es particularmente fructífera y permite predecir todas las posibles isomerismos según la naturaleza de los ligandos.
2. Estereoquímica estática y dinámica
La estereoquímica puede manifestarse en un aspecto dual, estático o dinámico.
2.1. Estereoquímica estática
La estereoquímica estática agrupa todos los datos relativos a la estructura de las moléculas, es decir, la ubicación en el espacio de los átomos entre sí. En muchos casos, la molécula no es rígida y su forma puede variar según la temperatura o la naturaleza de los sustituyentes. Estas variaciones, generalmente debidas a rotaciones alrededor de enlaces simples, se estudian mediante análisis conformacional. La estereoquímica permite predecir el número de estereoisómeros correspondientes a una fórmula estructural plana (o semiestructural) dada.
Se han desarrollado métodos para estudiar la estereoquímica de moléculas. Estos son esenciales en la química de los productos naturales para definir completamente la estructura de un compuesto que ha sido aislado. El interés de tal determinación no es puramente académico; las repercusiones son considerables si la sustancia tiene una actividad terapéutica, el conocimiento de su estructura posibilita entonces una síntesis parcial o total a escala industrial. Citemos el ejemplo de la cortisona: existen unos pocos miligramos en el mundo en 1945, el descubrimiento de su acción antiinflamatoria data de 1947, su síntesis parcial a partir de ácidos biliares se realiza a partir de 1950 en la escala del kilogramo.
2.2. Estereoquímica dinámica
La estereoquímica dinámica se refiere a la reactividad de las moléculas. El conocimiento del volumen espacial de una reacción significa que es necesario determinar la estereoquímica de los productos formados y definir la ruta de reacción, así como la geometría del estado de transición.
El control estérico en síntesis es muy importante; así, un compuesto (por ejemplo, penicilina) cuya fórmula plana comprende tres carbonos asimétricos (carbono unido a cuatro grupos de diferente naturaleza) puede existir en forma de 23 = 8 estereoisómeros distintos; pero solo un isómero tiene la actividad antibiótica deseada.
El estudio de la estereoquímica dinámica es un medio insustituible para obtener información muy precisa sobre los mecanismos de reacción (reacciones iónicas, radicales, fotoquímicas e incluso enzimáticas). Un ejemplo famoso es el de la inversión de Walden: ya en 1903, Paul Walden muestra, al trabajar con moléculas ópticamente activas, que ciertos casos de sustitución nucleofílica (denominada SN2) implican una inversión de configuración, por lo tanto una «inversión» del tetraedro inicial.
El estudio de la estereoquímica se basa en el hecho de que existen parámetros que pueden considerarse casi invariantes al pasar de un compuesto a otro. Por tanto, no es necesario empezar de cero para estudiar ningún compuesto nuevo. De hecho, las longitudes de los enlaces entre átomos, así como los ángulos formados por los enlaces entre ellos, varían muy poco de un compuesto a otro.
Los isómeros se denominan estereoisómeros cuando difieren solo en la disposición de sus átomos en el espacio. Debido a la naturaleza tetraédrica del carbono, surge el problema de la representación plana de una estructura tridimensional.
3. Los diferentes modos de representación
Se utilizan varios modos de representación: representaciones de Fischer, Cram, Newman … y cada uno de estos modos tiene sus propias convenciones que hay que respetar.
3.1. Representación de Fischer
La representación de Fischer es particularmente adecuada para la química de los carbohidratos, donde los aspectos estereoquímicos son importantes.
Los cuatro enlaces de un carbono saturado (→ química orgánica) están representados por líneas continuas, con la siguiente convención:
• una línea vertical corresponde a un enlace ubicado en el plano de la hoja o detrás de este plano;
• una línea horizontal corresponde a un enlace dirigido al frente del plano de la hoja.
• la cadena de carbono principal está ubicada verticalmente.
3.2. Representación de Cram
La representación de Cram de una molécula permite representarla en tres dimensiones sobre un soporte bidimensional. Muestra los enlaces de la molécula en perspectiva entre sí para comprender la estructura espacial de la molécula.
Los enlaces entre átomos se representan de la siguiente manera:
• enlace en el plano de la hoja:
• encuadernación delante del plano de la hoja:
• enlace detrás del plano de la hoja:
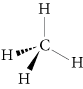
Por ejemplo, metano de fórmula CH4 tiene la siguiente representación de Cram:
3.3. Representación de Newman
La representación de Newman de un compuesto orgánico es su representación en papel que permite visualizar sus diferentes conformaciones (posiciones de los átomos de una molécula por rotación de enlaces simples carbono-carbono).
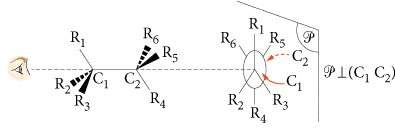
Para representar una molécula en una proyección de Newman debemos mirar la molécula en el eje de un enlace simple carbono-carbono, luego representamos los enlaces entre todos los átomos o grupos de átomos en un plano perpendicular al eje del carbono-carbono. vínculo.
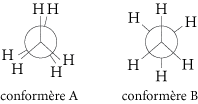
En general, la conformación más estable es aquella en la que los sustituyentes de los átomos de carbono ejercen las menores interacciones posibles entre sí, es decir, la conformación en la que están más distantes entre sí. Por ejemplo, en la representación de Newman de los confórmeros de etano en la posición eclipsada (conformador A) y desplazada (conformador B), el conformador más estable es el conformador B.
4. Estereoisomería
Se dice que una molécula es quiral (se pronuncia «kiral») si su imagen en relación con un espejo no puede superponerse a ella. Una molécula quiral no tiene centro ni plano de simetría. De lo contrario, se dice que es aquiral.
Una sustancia quiral siempre corresponde a un isómero estérico, su enantiómero.
Dos enantiómeros desvían en la dirección opuesta y en un ángulo igual el plano de un plano de luz polarizada; luego se mide la rotación óptica. Esta es la razón por la que hablamos deisomería óptica.
Son comunes las mezclas equimoleculares de enantiómeros. Se trata de las denominadas mezclas racémicas. El poder rotatorio de un racemato es cero como resultado de la compensación de las rotaciones de cada uno de los enantiómeros.
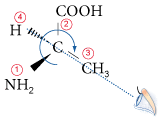
Se dice un carbono asimétrico cuando está vinculado a cuatro grupos de diferente naturaleza. Para distinguir los carbonos asimétricos entre sí, se utiliza una nomenclatura específica basada en su configuración: la nomenclatura R / S de Cahn, Ingold y Prelog. Por ejemplo, la configuración asimétrica de carbono de la analina es R (de recto, a la derecha porque los grupos giran en el sentido de las agujas del reloj).
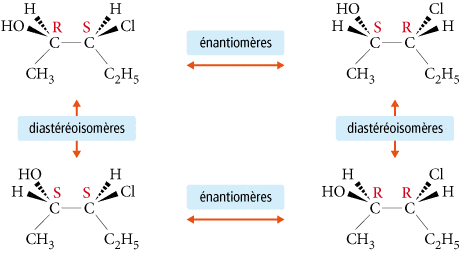
los diastereoisómeros son estereoisómeros configuracionales que no son enantiómeros (no son imágenes especulares entre sí). Pueden ser quirales o aquirales.
Las moléculas que contienen múltiples enlaces también pueden ser diastereómeros. Ejemplo: el ácido maleico (o ácido butenodioico) existe en dos configuraciones:
Para obtener más información, consulte el artículo. estereoisomería.