Una mezcla homogénea, también llamada solución, es aquella que tiene una sola fase, es decir, el soluto no es visible a simple vista. Las mezclas homogéneas pueden tener sus componentes separados principalmente a través de los siguientes procesos:
Destilación simple
Representa el proceso de fraccionamiento de solución más común en laboratorios e industrias químicas, donde se usa a menudo en la purificación de líquidos. Se utiliza, sobre todo, cuando se parte de una mezcla en la que uno de sus constituyentes es un sólido disuelto. Se basa en la marcada diferencia entre los puntos de ebullición (EP) entre ellos; el que tenga el PE más bajo destilará (pasará a la fase de vapor) primero.
En el proceso de destilación se observan dos fenómenos de carácter físico, el primero es la evaporación, donde la solución recibe energía térmica que se convertirá en la evaporación del componente con menor PE. La segunda es la condensación, cuando este componente vaporizado entrará en contacto con una superficie enfriada, volviendo a la fase líquida.
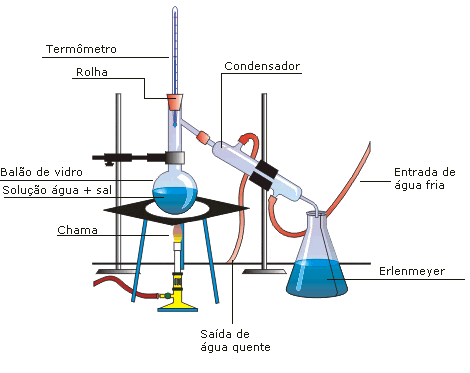
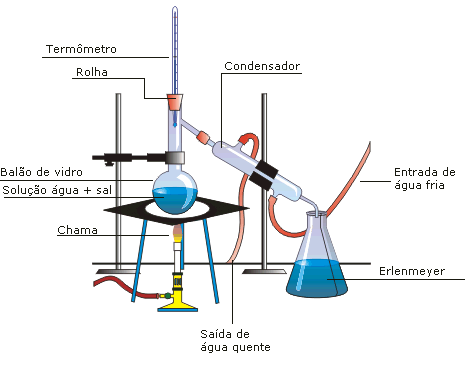
El esquema de una destilación simple se muestra a continuación:
En la figura anterior se muestran los instrumentos de laboratorio necesarios para el proceso. La mezcla puede ser, por ejemplo, una solución de cloruro de sodio (NaCl) y agua, en la que el primero (soluto) quedará retenido en el matraz, y el segundo (disolvente) se recogerá en el matraz Erlenmeyer.
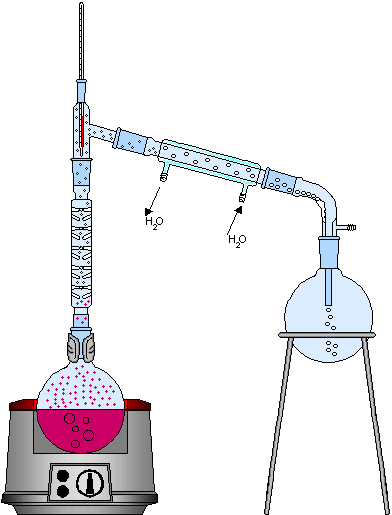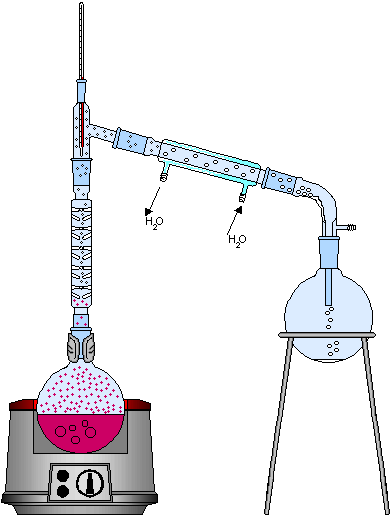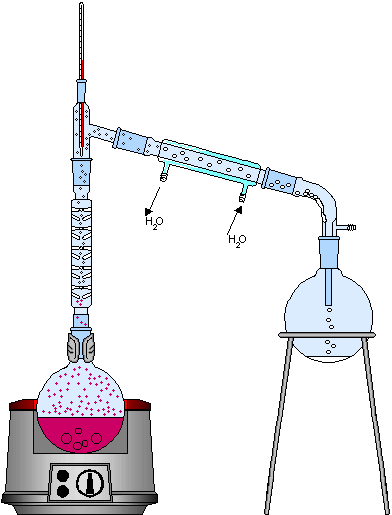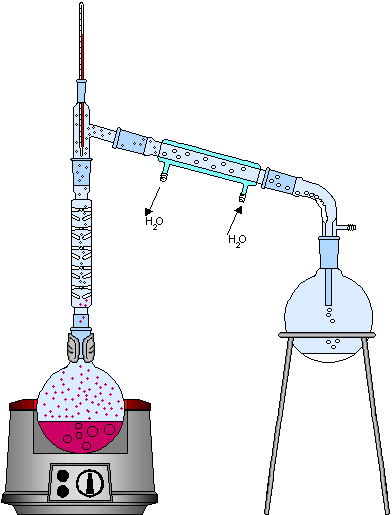
Cuando la mezcla homogénea está formada por dos líquidos, cuyos puntos de ebullición están más próximos que en el caso anterior, se hace necesario un proceso de destilación fraccionada. Este proceso se utiliza en la industria del refino de petróleo, donde algunos de sus componentes tienen puntos de ebullición cercanos; el proceso se representa a continuación:
Animación: http://www2.fc.unesp.br/lvq/animations.htm
La diferencia fundamental entre la instrumentación de una destilación simple y una destilación fraccionada es el uso en el segundo proceso de una columna de fraccionamiento, que tiene la función de incrementar la eficiencia del condensador, dificultando la mezcla de los líquidos a su salida.
Destilación de arrastre de vapor
Este proceso se basa en la extracción de sustancias que se descomponen a temperaturas cercanas a su punto de ebullición, y que no son solubles en agua o sus vapores. La relativa facilidad de descomposición de las sustancias impide el uso de procesos de destilación simple y fraccionada, por lo que es necesario “arrastrarlas” por agua vaporizada. El proceso, que se muestra a continuación, es muy común en la industria de las hierbas, en la extracción de componentes vegetales de las más diversas naturalezas.
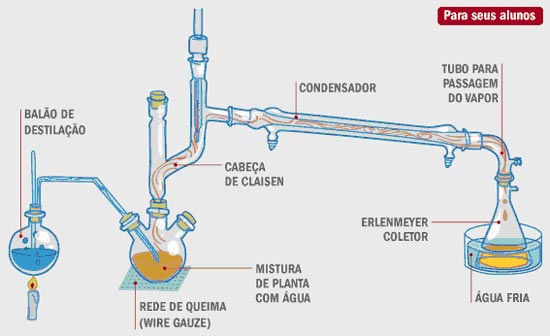
Se puede observar en la figura anterior que la instrumentación requerida en el proceso de arrastre de vapor es más detallada, requiriéndose dos fuentes de calor en lugar de una sola, como en los procesos anteriores. Al arrastrar vapor, se debe tener cuidado para que la segunda fuente de calor no degrade los componentes a extraer, pero tampoco condense la entrada de vapor de agua.
Referencias:
SARDELLA, Antonio; MATTHEW, Edegar; Curso de Química: química general, Ed. Ática, São Paulo / SP – 1995.
MAHAN, Bruce M .; MYERS, Rollie J .; Química: un curso universitario, Ed. Edgard Blucher LTDA, São Paulo / SP – 2002